
Ⅰ. 在实验室利用下列装置,可制备某些气体并验证其化学性质。
完成下列表格:
| 序号 | 气体 | 装置连接顺序(填字母) | 制备反应的化学方程式 |
| (1) | 乙烯 | _________________ | _________________ |
| (2) | 乙炔 | A→C→E | _________________ |

 =_______________。
=_______________。 (12分,每空2分)Ⅰ.(1)B→D→E 
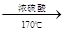
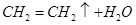
(2)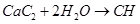
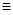

Ⅱ. (1)A、B、D、E、F;(2)饱和食盐水 (3)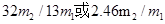
解析试题分析:Ⅰ.①实验室制取乙烯利用的是乙醇在浓硫酸的作用下加热到170℃通过消去反应制备乙烯。由于生成的乙烯中含有SO2,所以在通过酸性高锰酸钾溶液检验乙烯的性质之前,要首先除去SO2,所用试剂是氢氧化钠溶液,即连接顺序是B→D→E ,反应的方程式是
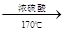
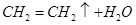 。
。
②实验室制取乙炔,利用的是电石和饱和食盐水反应制备,反应的方程式是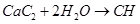
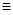
 。
。
Ⅱ. (1)测定电石样品的纯度,则可以通过测量电石与水反应生成的乙炔来完成。由于乙炔能被溴的四氯化碳溶液吸收,通过称量反应前后的质量即可得出生成的乙炔质量。但由于生成的乙炔气体中含有H2S和PH3,所用需要分别通过浓硫酸和硫酸铜除去。又因为装置中含有没有被完全排出的气体,因此还需要借助于A装置,因此正确的连接顺序是A、B、D、E、F。
(2)为保证测定的精度,要求产生乙炔的气流较为平缓,在分液漏斗中应装入的液体是饱和食盐水。
(3)F吸收乙炔前后的质量差为m2g,则生成的乙炔质量就是m2g,所用根据方程式可知碳化钙的质量是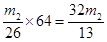 ,因此电石样品中CaC2质量分数
,因此电石样品中CaC2质量分数 =
=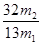 。
。
考点:考查乙烯、乙炔的实验室制备、电石纯度测定的实验探究
点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力,提高学生的学科素养。该类试题综合性强,理论和实践的联系紧密,有的还提供一些新的信息,这就要求学生必须认真、细致的审题,联系所学过的知识和技能,进行知识的类比、迁移、重组,全面细致的思考才能得出正确的结论。


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:实验题
CaCO3广泛存在于自然界,是一种重要的化工原料。大理石主要成分为CaCO3,另外有少量的含硫化合物(如FeS等)。实验室用大理石和稀盐酸反应制备CO2气体。下列装置可用于CO2气体的提纯和干燥。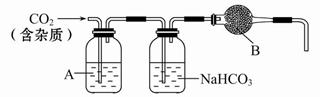
完成下列填空:
(1)用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1),应选用的仪器是_____。
a.烧杯 b.玻璃棒 c.量筒 d.容量瓶
(2)上述装置中,A是_____溶液,NaHCO3溶液可以吸收_____。
(3)上述装置中,B物质是_____。把这个实验得到的气体收集起来,用来测定CO2的分子量,如果B物质失效,测定结果_____(填“偏高”、“偏低”或“不受影响”)。
(4)一次性饭盒中石蜡(高级烷烃)和CaCO3在食物中的溶出量是评价饭盒质量的指标之一,测定溶出量的主要实验步骤设计如下:
剪碎、称重→浸泡溶解→过滤→残渣烘干→冷却、称重→恒重,为了将石蜡溶出,应选用的试剂是_____,碳酸钙溶出,应选用的试剂是_____。
a.氯化钠溶液 b.稀醋酸
c.稀硫酸 d.正己烷
(5)在溶出量测定实验中,为了获得石蜡和碳酸钙的最大溶出量,应先溶出_____,原因是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
选用适当装置、试剂和方法可制备中学化学中的几种常见气体。请填写表中的空格(从①~⑩中选择,填序号):
| 实验 | 气体 | 所用装置 | 气体性质 | 干燥该气体选用的试剂 |
| (1) | | ③ | 其水溶液显碱性 | |
| (2) | | | 1mol最多能与2molH2反应 | ⑩ |

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
已知用P2O5作催化剂,加热乙醇可制备乙烯,反应温度为80℃~210℃。某研究性小组设计了如下的装置制备并检验产生的乙烯气体(夹持和加热仪器略去)。

(1)仪器a的名称为_________________
(2)用化学反应方程式表示上述制备乙烯的原理______________________________。
(3)已知P2O5是一种酸性干燥剂,吸水放大量热,在实验过程中P2O5与乙醇能发生作用,因反应用量的不同,会生成不同的磷酸酯,它们均为易溶于水的物质,沸点较低。写出乙醇和磷酸反应生成磷酸二乙酯的化学方程式(磷酸用结构式表示为 )__________________________________。
)__________________________________。
(4)某同学认为用上述装置验证产生了乙烯不够严密,理由是___________________。
(5)某同学查文献得知:40%的乙烯利(分子式为C2H6ClO3P)溶液和NaOH固体混和可快速产生水果催熟用的乙烯,请在上述虚线框内画出用乙烯利溶液和NaOH固体制取乙烯的装置简图(夹持仪器略)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
不久前,一则“食用撒了鱼浮灵的鱼虾可能致癌”的微博在网上热传。“鱼浮灵”的化学成分实为过碳酸钠,使用不当会让鱼损伤,过碳酸钠本身无毒无害,对人体不会有危害。过碳酸钠,俗称固体双氧水,化学式为2Na2CO3·3H2O2,是一种无机盐,是白色颗粒状粉末,可以分解为碳酸钠和过氧化氢。某探究小组制备过碳酸钠并测定样品中H2O2的含量,其制备流程和装置示意图如下:
已知:50 °C时 2Na2CO3·3H2O2 (s) 开始分解
主反应 2Na2CO3 (aq) + 3H2O2 (aq) 2Na2CO3·3H2O2 (s) ΔH < 0
2Na2CO3·3H2O2 (s) ΔH < 0
副反应 2H2O2 = 2H2O + O2↑
滴定反应 6KMnO4 + 5(2Na2CO3·3H2O2) +19H2SO4 = 3K2SO4 + 6MnSO4+10Na2SO4 + 10CO2 ↑ + 15O2↑ + 34H2O
根据以上信息回答下列问题:
(1)推测图中支管的作用可能是 。
(2)步骤①的关键是控制温度,结合装置图归纳其措施有 、
和 。
(3)在滤液X中加入适量NaCl固体或无水乙醇均可析出过碳酸钠,原因是 。
(4)步骤③中选用无水乙醇洗涤产品的目的是 。
(5)测定样品中H2O2的质量分数的方法是:准确称取0.2000g过碳酸钠样品于250 mL 锥形瓶中,加50 mL 蒸馏水溶解,再加50 mL 2.000 mol·L-1 H2SO4 (H2SO4过量),用0.002000mol·L-1 KMnO4标准溶液滴定至终点时消耗30.00 mL。
①滴定前,滴定管需用KMnO4标准溶液润洗2~3次,润洗的操作方法是:关闭酸式滴定管活塞,向滴定管中注入少量KMnO4标准 。
②上述样品中H2O2的质量分数计算表达式为 (只列出算式,不作任何运算!H2O2的式量为34.00)。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
无水氯化铝是白色晶体,易吸收水分,在178℃升华,装有无水氯化铝露置于潮湿空气中会爆炸并产生大量白雾,工业上由金属与氯气作用或由无水氯化氢气体与熔融Al作用而制得,某课外活动小组在实验室内通过下列装置(如下图)制取少量纯净的无水氯化铝。
试回答以下问题:
(1)装置A中反应的化学方程式
(2)为使实验成功,A和B间需要加适当的装置,请将它画在框内,并注明其中盛放的药品。如果A产生的气体直接进入B中,实验产生的不良后果是 。
(3)进行实验时,应先点燃(填写字母,下同) 处的酒精灯,然后再点燃
处的酒精灯。
(4)在C处可以收集到纯净的氯化铝,原因是 。
(5)装置D的作用是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列实验操作不能达到预期实验目的的是
| | 实验目的 | 实验操作 |
| A | 鉴别乙酸乙酯和乙酸 | 分别加入饱和Na2CO3溶液 |
| B | 比较Fe和Cu的金属活动性 | 分别加入浓硝酸 |
| C | 比较H2O和乙醇中羟基氢的活泼性 | 分别加入少量Na |
| D | 比较I2在H2O和CCl4中的溶解度 | 向I2水中加入CCl4,振荡 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图所示的实验,能达到实验目的的是
| A | B | C | D |
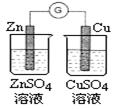 |  |  |  |
| 验证化学能转化为电能 | 验证温度对平衡移动的影响 | 验证铁发生析氢腐蚀 | 验证非金属性Cl> C > Si |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列对实验现象的解释与结论,正确的是( )
| 选项 | 实验操作 | 实验现象 | 解释与结论 |
| A | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液 | 有白色沉淀产生 | 蛋白质发生了变性 |
| B | 向某溶液中加入盐酸酸化的BaCl2溶液 | 有白色沉淀产生 | 该溶液中一定含有SO42- |
| C | 向甲苯中滴入少量浓溴水,振荡,静置 | 溶液分层,上层呈橙红色,下层几乎无色 | 甲苯和溴水发生取代反应,使溴水褪色 |
| D | 向蔗糖中加入浓硫酸 | 变黑,放热,体积膨胀,放出刺激性气体 | 浓硫酸具有脱水性和强氧化性,反应中生成C、SO2和CO2等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com