
【题目】下列分子中,所有碳原子一定在同一平面上的是
A. CH3-CH2-CH2-CH3B. CH3-CH=CH-CH2-CH3
C. ![]() D. CH3-C
D. CH3-C![]() C-CH3
C-CH3
科目:高中化学 来源: 题型:
【题目】以镁渣[含有MgCO3、Mg(OH)2、CaCO3、Al2O3、Fe2O3和SiO2]为原料制取六水合氯化镁(MgCl2·6H2O),具体的工艺流程如图:

已知:①滤液2与适量石灰乳反应合成碱式氯化镁[Mg(OH)2-xClx·mH2O],当x=1,m=0时,碱式氯化镁为Mg(OH)Cl。
②相关金属离子[c(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下表:
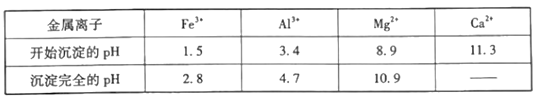
请回答下列问题:
(1)实验室煅烧样品的实验仪器为__。
(2)滤渣2的主要成分是__。
(3)通过调节滤液2的pH来获取Mg(OH)2沉淀,则溶液pH的范围为___。
(4)向溶液A中先加入___(填化学式)酸化,然后___、冷却结晶、过滤、洗涤和低温干燥得到MgCl2·6H2O,取少量低温干燥得到的MgCl2·6H2O晶体溶于水后发现溶液呈碱性,则含有的杂质是__从操作上分析引入杂质的原因是__。
(5)热重分析法是程序控制温度下测最物质的质量与温度关系的一种实验技术。MgCl2·6H2O的热重曲线如图。已知:MgCl2·6H2O在空气中受热脱水时,不产生无水氯化镁。

①试确定200℃时固态物质的化学式:___。
②温度升至554℃时分解得到的主要产物为白色固体和一种酸性气体,写出该反应的化学方程式:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示的是纯净物、单质、化合物、含氧化合物、氧化物、碱之间的包含、不包含关系,若整个大圆圈代表纯净物,则下列选项中,能正确指出①、②、③、④、⑤所属物质类别的是( )
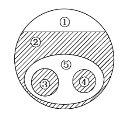
A. ①单质、③化合物
B. ②碱、⑤氧化物
C. ④碱、⑤含氧化合物
D. ④含氧化合物、③氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 乳酸薄荷醇酯(![]() )仅能发生水解、氧化、消去反应
)仅能发生水解、氧化、消去反应
B. 乙醛和丙烯醛(![]() )不是同系物,它们与氢气充分反应后的产物也不是同系物
)不是同系物,它们与氢气充分反应后的产物也不是同系物
C. 淀粉和纤维素在酸催化下完全水解后的产物都是葡萄糖
D. CH3COOCH2CH3与CH3CH2COOCH3互为同分异构体,1H-NMR谱显示两者均有三种不同的氢原子且三种氢原子的比例相同,故不能用1H-NMR来鉴别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物X是一种药物合成的中间体,其结构简式如图所示。下列有关化合物X的说法正确的是( )
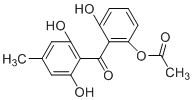
A.化合物X不能使酸性高锰酸钾溶液褪色
B.1mol化合物X最多可与5 mol NaOH、4 mol Br2发生反应
C.能发生加成反应、取代反应、氧化反应、消去反应
D.化合物X中含有10种化学环境不同的氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知10.4 g某有机物X在空气中完全燃烧,所得产物先后通过足量的浓硫酸和碱石灰,分别增重7.2克和35.2克。物质X在不同条件下能发生如下图所示的一系列变化。

注:CH3—CH=CH2+HBr→CH3—CHBr—CH3(主要产物)
(1)X的化学式:________,X的结构简式:________ ,C的结构简式:______。
(2)上述反应中,①是________反应,⑦是________反应。(填反应类型)
(3)写出D→E反应的化学方程式_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组将纯净的SO2气体通入0.1mol·L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀,为探究上述溶液中何种微粒能氧化通入的SO2,该小组突出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一
该小组涉及实验验证了假设一,请在下表空白处填写相关实验现象
实验步骤 | 实验现象 | 结论 |
实验1:在盛有不含O2的25ml0.1mol/LBaCl2溶液的烧杯中,缓慢通入纯净的SO2气体 | ____ | 假设一成立 |
实验2:在盛有不含O2的25ml0.1mol/LBa(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体 | ____ |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线入下图
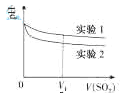
实验1中溶液pH变小的原因是____;V1时,实验2中溶液pH小于实验1的原因是(用离子方程式表示)_________。
(3)验证假设二
请设计实验验证假设二,写出实验步骤,预期现象和结论。
实验步骤、预期现象和结论(不要求写具体操作过程)____
(4)若假设二成立,请预测:在相同条件下,分别通入足量的O2和KNO3,氧化相同的H2SO3溶液(溶液体积变化忽略不计),充分反映后两溶液的pH前者_______(填大于或小于)后者,理由是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黑火药是我国古代的四大发明之一。黑火药爆炸时发生的反应为:2KNO3+S+3C=K2S+N2↑+3CO2↑。回答下列问题:
(1)基态钾原子的核外电子排布式为____________,第一电离能:K______ (填“>”或“<”)Na。
(2)NO3-的空间构型为_____________。
(3)固态硫易溶于CS2,熔点为112℃,沸点为444.8℃。其分子结构为 ,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
,S8中硫原子的杂化轨道类型是____________,S8分子中至多有________个硫原子处于同一平面。
(4)N2分子中σ键与π键的个数比为________,N2的沸点比CO的沸点____(填“高”或“低”)。
(5)K2S的晶胞结构如图所示。其中K+的配位数为_______,S2-的配位数为____;若晶胞中距离最近的两个S2-核间距为a cm,则K2S晶体的密度为____g·cm-3(列出计算式,不必计算出结果)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是
A.BeCl2为V形的极性分子
B.ClO4的空间构型为正四面体形
C.P4和CH4都是正四面体分子且键角都为109°28′
D.H2O和CO32的中心原子均为sp3杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com