


 .
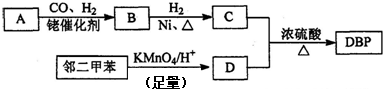
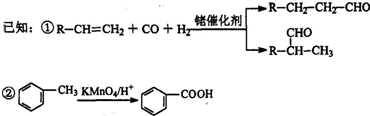
. 分析 A是烃,A的质谱图表明其相对分子质量为42,红外光谱表明分子中含有碳碳双键,则A为CH3CH=CH2;A发生信息中醛的加成反应生成B,且B能发生银镜反应,结合B与氢气发生加成反应生成C,有机物C的核磁共振氢谱显示其分子中含有5种化学环境不同的氢原子,且个数之比为3:2:2:2:1,则B为CH3CH2CH2CHO,C为CH3CH2CH2CH2OH,邻二甲苯发生氧化反应生成D为 ,C与D发生酯化反应生成DBP为
,C与D发生酯化反应生成DBP为 ,据此分析解答.
,据此分析解答.
解答 解:A是烃,A的质谱图表明其相对分子质量为42,红外光谱表明分子中含有碳碳双键,则A为CH3CH=CH2;A发生信息中醛的加成反应生成B,且B能发生银镜反应,结合B与氢气发生加成反应生成C,有机物C的核磁共振氢谱显示其分子中含有5种化学环境不同的氢原子,且个数之比为3:2:2:2:1,则B为CH3CH2CH2CHO,C为CH3CH2CH2CH2OH,邻二甲苯发生氧化反应生成D为 ,C与D发生酯化反应生成DBP为
,C与D发生酯化反应生成DBP为 ,
,
(1)A为CH3CH=CH2,A的名称为丙烯;
CH3CH=CH2在一定条件下发生加聚反应生成聚丙烯,聚丙烯的结构简式: ,
,
故答案为:丙烯; ;
;
(2)D为 ,D中的含氧官能团是羧基,有机物D和足量有机物C反应生成DBP的反应是CH3CH2CH2CH2OH与邻苯二甲酸发生酯化反应,反应的方程式为:
,D中的含氧官能团是羧基,有机物D和足量有机物C反应生成DBP的反应是CH3CH2CH2CH2OH与邻苯二甲酸发生酯化反应,反应的方程式为: ,
,
故答案为:羧基; ;
;
(3)a.A为CH3CH=CH2,含有碳碳双键,能发生聚合反应、加成反应和氧化反应,故a正确;
b.C为CH3CH2CH2CH2OH,与C互为同分异构体,且含有相同官能团的有机物有CH3CH2CH(OH)CH3、(CH3)2C(OH)CH3种、(CH3)2CHCH2(OH)3种,故b错误;
c.因为在烷烃中甲基不能被酸性高锰酸钾氧化,而邻二甲苯能氧化生成D,所以说明有机物分子中基团之间存在影响,故c正确;
d.1mol DBP可与含2mol NaOH的溶液完全反应,故d错误;
故选:ac;
(4)D为 ,D的同分异构体符合下列条件:
,D的同分异构体符合下列条件:
①属于酚类化合物,说明含有酚羟基;
②能与NaHCO3溶液反应,说明含有羧基;
③能发生银镜反应说明含有-CHO;
如果-CHO、-OH、-COOH三种官能团,且-CHO、-OH位于邻位,有4种结构,
如果-CHO、-OH、-COOH三种官能团,且-CHO、-OH位于间位,有4种结构,
如果-CHO、-OH、-COOH三种官能团,且-CHO、-OH位于对位,有邻间对2种结构,
所以符合条件的有10种同分异构体,故答案为:10;
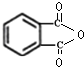
(5)根据中间产物+C$\stackrel{浓硫酸}{→}$DBP+H2O,则中间产物为: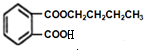 ,又根据E+C$\stackrel{浓硫酸}{→}$中间产物以及E(C8H403),则E为:
,又根据E+C$\stackrel{浓硫酸}{→}$中间产物以及E(C8H403),则E为: ,故答案为:
,故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断及知识迁移能力,根据流程图中反应条件、结合题给信息采用知识迁移的方法进行推断,难点是(4)题同分异构体种类判断,题目难度中等.


科目:高中化学 来源:2017届吉林省长春市高三上学期期中考试化学试卷(解析版) 题型:选择题
下列关于物质分类的说法正确的是
①稀豆浆、硅酸、氯化铁溶液都属于胶体
②HF、HI都属于弱电解质
③Na2O、MgO、Al2O3均属于碱性氧化物
④明矾、冰醋酸、四氧化三铁都不是混合物
⑤葡萄糖、油脂都不属于有机高分子化合物
A.④⑤
B.②④
C.①②
D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PM2.5(直径小于或者等于2.5×10-6m的细颗粒物)分散在空气中形成的溶胶 | |
| B. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 | |
| C. | 自来水厂可使用Cl2和绿矾(FeSO4•7H2O) 进行自来水的消毒、净化,以改善水质 | |
| D. | 在食品包装袋中放入装有硅胶的透气小袋,可以防止食物氧化变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
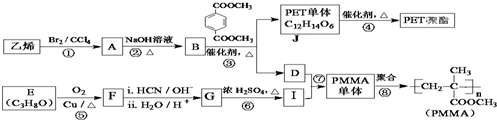
 $→_{ii.H_{2}O/H+}^{i.HCN/OH-}$
$→_{ii.H_{2}O/H+}^{i.HCN/OH-}$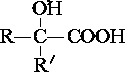 (R、R′代表烃基)
(R、R′代表烃基) $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.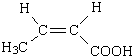 .
.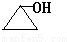 、
、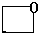 、
、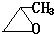 .
.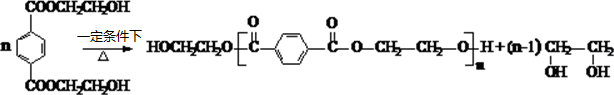 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 微粒半径:Cl->K+>Al3+>O2- | B. | 碱性:KOH>Ca(OH)2>Mg(OH)2 | ||
| C. | 晶体熔点:金刚石>氯化镁>汞>碘 | D. | 稳定性和还原性:H2O>H2S>AsH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | W分别与X、Y形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物的水化物的酸性比Z的弱 | |
| D. | Z的简单氢化物的热稳定性比W的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,B、C、D、E与A形成的化合物中稳定性最强的是H2O(填化学式).
,B、C、D、E与A形成的化合物中稳定性最强的是H2O(填化学式).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com