
【题目】《唐本草》是我国唐代中药学著作,记载药物844种,其中有关于“青矾”制“绛矾”的过程描述为:“…本来绿色,新出窟未见风者,正如瑠璃…烧之赤色…”据此推测,“青矾”的主要成分是下列中的
A. CuSO4·5H2O B. FeSO4·7H2O C. KAl(SO4)2·12H2O D. MgSO4·7H2O
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 分子的结构是由键角决定的
B. 共价键的键能越大,共价键越牢固,由该键形成的分子越稳定
C. CF4、CCl4、CBr4、CI4中C—X键的键长、键角均相等
D. H2O分子中两个O—H键的键角为180°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,由水电离出的 c(H+) = 10-11mol/L 溶液中,一定能大量存在的离子是( )
A. Fe3+ B. CH3COO- C. HCO3- D. NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现,烯烃在合适的催化剂作用下双键可断裂,两端基团重新组合为新的烯烃若CH2===C(CH3)CH2CH3与CH2===CHCH2CH3的混合物发生该类反应,则新生成的烯烃的种数是(包括顺反异构)
A. 5 B. 6 C. 7 D. 8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的化工原料,是氯碱工业的主要产品之一,它是一种常用的消毒剂。
①实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是______________________
②氯碱工业生产氯气的化学方程式为______________________
③由于氯气贮存运输不方便,工业上常将氯气转化为漂白粉,工业上生产漂白粉的主要化学方程式是______________________,在空气中漂白粉长期存放会变质而失效的原理是(用化学方程式说明) _____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如右图所示。则下列离子组在对应的溶液中,一定能大量共存的是( )
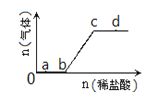
A.a点对应的溶液中:Na+、OH-、SO42-、NO3-
B.b点对应的溶液中:Al3+、Fe3+,MnO4-、Cl-
C.c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
D.d点对应的溶液中:F-、NO3-、Fe2+、Ag+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用菱锰矿(主要含MnCO3、FeCO3、Al2O3、SiO2)制备MnSO4·H2O的工艺流程如下:
Ⅰ.向菱锰矿中加入过量稀H2SO4,过滤;
Ⅱ.向滤液中加入过量MnO2,过滤;
Ⅲ.调节滤液pH=a,过滤;
Ⅳ.浓缩、结晶、分离、干燥得到产品;
Ⅴ.检验产品纯度。
(1)步骤Ⅰ中,滤渣的主要成分是 。
(2)将MnO2氧化Fe2+的离子方程式补充完整:
MnO2 + ![]() Fe2+ +
Fe2+ +![]() =
=![]() Mn2+ +
Mn2+ + ![]() Fe3+ +
Fe3+ +![]()
(3)与选用Cl2作为氧化剂相比,MnO2的优势主要在于:原料来源广、成本低、可避免环境污染、 。
(4)已知:生成氢氧化物沉淀的pH
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Mn(OH)2 | |
开始沉淀时 | 3.4 | 6.3 | 1.5 | 7.6 |
完全沉淀时 | 4.7 | 8.3 | 2.8 | 10.2 |
注:金属离子的起始浓度为0.1mol/L
步骤Ⅲ中a的取值范围是 。
(5)步骤Ⅴ,通过测定产品中锰元素的质量分数来判断产品纯度。
已知一定条件下,MnO4-与Mn2+反应生成MnO2 。取x g产品配成溶液,用0.1mol/L KMnO4溶液滴定,消耗KMnO4溶液y mL,产品中锰元素的质量分数为 (用含x、y表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类的正确组合是( )
选项 | 酸 | 碱 | 碱性氧化物 | 盐 |
A | H2CO3 | 纯碱 | CaO | 明矾 |
B | H2SO4 | 烧碱 | Na2O | 小苏打 |
C | HNO3 | 氨水 | Al2O3 | 石灰石 |
D | NaHCO3 | 熟石灰 | Al(OH)3 | 食盐 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com