
【题目】(1)反应A(g)+B(g)![]() C(g)+D(g)过程中的能量变化如图所示,回答下列问题。
C(g)+D(g)过程中的能量变化如图所示,回答下列问题。

①该反应是____反应(填“吸热”、“放热”)。
②当反应达到平衡时,升高温度,A的转化率___(填“增大”、“减小”、“不变”),原因是____。
③反应体系中加入催化剂对反应热是否有影响?____(填“有”、“无”),原因是____。
④在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1____,E2____(填“增大”、“减小”、“不变”)。
(2)已知由氢气和氧气反应生成1 mol水蒸气,放出241.8kJ热量。
①写出该反应的热化学方程式___。
②若1g水蒸气转化成液态水放热2.494kJ,则反应H2(g)+1/2O2(g)=H2O(l)的ΔH=_kJ·mol-1。
【答案】放热 减小 该反应正反应是放热反应,升高温度平衡向逆反应移动 无 催化剂不改变反应物总能量与生成物总能量之差即反应热不变 减小 减小 H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8kJ·mol-1 -286.7
【解析】
(1)①根据图像可知,反应物的总能量大于生成物的总能量;
②正反应为放热反应,根据勒夏特列原理进行推理;
③催化剂能降低反应的活化能,对反应物及生成物的总能量无影响;
④催化剂能降低反应的活化能;
(2)①生成1 mol水蒸气时,氢气为1mol,氧气为0.5mol计算热化学方程式的焓变;
②1g水为1/18mol,则1mol水蒸汽生成液体水时释放能量=2.494kJ×18=44.892kJ,则热方程式为H2O(g)= H2O(l) ΔH=-44.892kJ/mol,根据盖斯定律计算焓变。
(1)①根据图像可知,反应物的总能量大于生成物的总能量,反应为放热反应;
②正反应为放热反应,根据勒夏特列原理,升高温度,平衡逆向移动,A的反应量减少,转化率减小;
③催化剂能降低反应的活化能,对反应物及生成物的总能量无影响,则对反应热无影响;
④催化剂能降低反应的活化能,则E1减小,反应的焓变不变,则E2减小;
(2)①生成1 mol水蒸气时,氢气为1mol,氧气为0.5mol,则热化学方程式为H2(g)+1/2O2(g)=H2O(g) ΔH=-241.8kJ/mol;
②1g水为1/18mol,则1mol水蒸汽生成液体水时释放能量=2.494kJ×18=44.892kJ,则热方程式为H2O(g)= H2O(l) ΔH=-44.892kJ/mol,根据盖斯定律,两式相加可得H2(g)+1/2O2(g)=H2O(l),则ΔH=-241.8kJ/mol-44.892kJ/mol=-286.7 kJ/mol。


 导学教程高中新课标系列答案
导学教程高中新课标系列答案科目:高中化学 来源: 题型:
【题目】小王要制备纯净的二氧化碳气体,可供选用的仪器如图所示。可供选用的药品如下:①石灰石②澄清石灰水③稀硫酸④浓硫酸⑤盐酸溶液⑥烧碱溶液⑦蒸馏水。下列装置连接顺序及组合最恰当的是( )

A. A(①⑤)、B(④)、C(⑦)、DB. A(①③)、B(④)、C(⑦)、D
C. A(①⑤)、B(⑦)、C(④)、DD. A(①⑤)、B(⑥)、C(④)、D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A(g)+B(g)![]() C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ | 700 | 900 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
回答下列问题:
(1)该反应的平衡常数表达式K=____________,△H____0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003 mol·L-1·s-1。则6s时c(A)=_____mol·L-1, C的物质的量为______mol;若反应经一段时间后,达到平衡时A的转化率为_____,如果这时向该密闭容器中再充入1 mol氩气,平衡时A的转化率为_________;
(3)判断该反应是否达到平衡的依据为______(填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g)![]() A(g)+B(g)的平衡常数的值为_____________。
A(g)+B(g)的平衡常数的值为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中和热ΔH=57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热ΔH=2×(57.3)kJ/mol
B.CO(g)的燃烧热是ΔH=283.0kJ/mol,则2CO(g)+O2(g)=2CO2(g)反应的ΔH=(2×283.0)kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三种气体X、Y、Z的相对分子质量关系为Mr(X) < Mr(Y)= 0.5Mr(Z),下列说法正确的是()
A.原子数目相等的三种气体,质量最大的是Z
B.相同条件下,同质量的三种气体,气体密度最小的是X
C.若一定条件下,三种气体体积均为2.24 L,则它们的物质的量一定均为0.1 mol
D.同温下,体积相同的两容器分别充2gY气体和1gZ气体,则其压强比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置(部分夹持装置已略去)可以达到对应实验目的的是
A.制备氢氧化铁胶体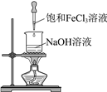 B.分离乙酸乙酯和饱和Na2CO3溶液
B.分离乙酸乙酯和饱和Na2CO3溶液
C.除去CO2中的少量HCl  D.收集NO2
D.收集NO2 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有__________________________________;
(2)硫酸铜溶液可以加快氢气生成速率的原因是____________________________;
(3)实验室中现有![]() 、
、![]() 、
、![]() 、
、![]() 等4中溶液,可与实验中
等4中溶液,可与实验中![]() 溶液起相似作用的是______________________________________;
溶液起相似作用的是______________________________________;
(4)要加快上述实验中气体产生的速率,还可采取的措旌有________(答两种);
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
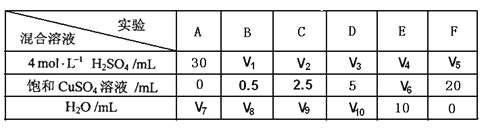
①请完成此实验设计,其中:V1=______,V6=______,V9=______;
②该同学最后得出的结论为:当加入少量![]() 溶液时,生成氢气的速率会大大提高。但当加入的
溶液时,生成氢气的速率会大大提高。但当加入的![]() 溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因________________________________________________________
溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用如图装置制取一定量的饱和氯水,并进行氯水的性质实验。
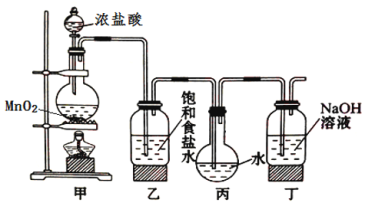
(1)在装入药品前应进行的操作____________________________________________。
(2)写出丁装置中发生反应的离子方程式:_______________________。
(3)用制得的饱和氯水分别进行下列实验:
①滴入碳酸钠溶液中,有气体生成,说明氯水中发生反应的粒子是___________;
②滴到蓝色石蕊试纸上的现象:_________________________________________。
(4)久置的氯水漂白效果明显不足或消失,用化学方程式表示:_________________。
(5)将制得的饱和氯水慢慢滴入含有酚酞的NaOH稀溶液中,当滴到一定量时,红色突然褪去。产生上述现象的原因可能有两种(简要文字说明):
①__________________________________________________________________;
②__________________________________________________________________。
用实验证明红色褪去的原因是①或者②的实验方法是:___________。
(6)科学家提出,使用氯气对自来水消毒时,氯气会与水里的有机物反应,生成的有机氯化物可能对人体有害,现已开始使用新的自来水消毒剂,如_________________(举两例,写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
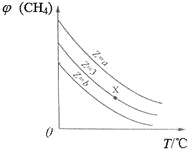
A. 该反应的焓变ΔH>0
B. 图中Z的大小为a>3>b
C. 图中X点对应的平衡混合物中![]() =3
=3
D. 温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com