
【题目】下列有关实验的说法错误的是( )
A.将一小块试纸放在表面皿上,用玻璃棒蘸取少量待测液点在试纸上,再与标准比色卡对照
B.无色溶液中加Ba(NO3)2溶液,再加稀盐酸,沉淀不溶解,不能说明原溶液中一定有SO42﹣
C.蒸馏时蒸馏烧瓶中液体的体积不能超过容积的 ![]() ,液体也不能蒸干
,液体也不能蒸干
D.将固体加入容量瓶中溶解并稀释至刻度,配制成一定物质的量浓度的溶液
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol/L NaOH溶液分别滴定20.00 mL 0.1000 mol/L盐酸和20.00 mL 0.1000 mol/L醋酸溶液,得到2条滴定曲线,如下图所示:
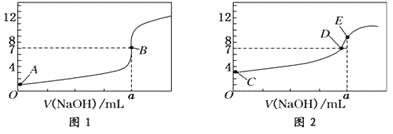
以HA表示酸,下列说法正确的是( )
A. 滴定盐酸的曲线是图2
B. 达到B、D状态时,两溶液中离子浓度均为c(Na+)=c(A—)
C. 达到B、E状态时,反应消耗的n( CH3COOH)>n(HCl)
D. 当0mL< V(NaOH)<20.00mL时,对应混合溶液中各离子浓度由大到小的顺序均为c(A-)>c(Na+)>c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验,将乙醇与浓硫酸的混合液加热至170℃,将生成的气体通入溴水中,发现溴水褪色,即证明乙烯与溴水发生了加成反应.
(1)写出甲同学实验中两个主要的化学方程式_______________;___________;
(2)乙同学在甲同学的实验中发现,生成的气体有刺激性气味,推测产生的气体除乙烯外,还有副产物SO2 和CO2,SO2也能使溴水褪色:SO2+Br2+2H2O→H2SO4+2HBr
于是对甲同学的结论提出质疑;为确认乙烯能使溴水褪色,甲同学在实验时先将混合气体通过足量的_________(填序号)以除去其中的SO2,再通入溴水时发现剩余气体仍能使溴水褪色.
(A)氯水 (B)NaOH溶液 (C)酸性KMnO4溶液
(3)乙同学又提出质疑,认为乙烯使溴水褪色也可能发生了取代反应:CH2=CH2+Br2→CH2=CHBr+HBr
甲同学认为很有道理,于是又做了一个简单的实验来确认是否发生取代反应,该实验所用的试剂是_________,可能的现象和结论是______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于硅及其化合物的叙述错误的是
A. 生产普通玻璃和水泥都用到石灰石
B. 硅是光导纤维的基本原料
C. 赏心悦目的雕花玻璃是用氢氟酸对玻璃进行刻蚀而制成的
D. 硅酸凝胶经干燥脱水可得硅胶,硅胶可作瓶装药品的干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.“量子化”就是不连续的意思,微观粒子运动均有此特点
B.英国科学家道尔顿首先发现了电子
C.焰色反应与电子跃迁有关,属于化学变化
D.基态氢原子转变成激发态氢原子时释放能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A.具有规则几何外形的固体一定是晶体
B.晶体与非晶体的根本区别在于是否具有规则的几何外形
C.具有各向异性的固体一定是晶体
D.晶体、非晶体都具有固定的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。其部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解,产生大量白雾 ②易分解:SO2Cl2 |
回答下列问题:
Ⅰ.实验室合成硫酰氯要先制取干燥氯气。制备干燥纯净的氯气所用仪器如下图:

(1)圆底烧瓶中发生的离子反应方程式为_____________。
(2)上述仪器的连接顺序是:e接 , 接 , 接 , 接 (按气流方向,用小写字母表示)。______________________
II.催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):

(3)仪器B冷却水的进口为________(填“a””或“b”),活性炭的作用是________。
(4)装置D除干燥气体外,另一作用是_______________。若缺少D,则硫酰氯会水解,该反应的化学方程式为________________。
(5)某同学建议将收集器A放在冰水中冷却,你认为该同学的建议是否合理,为什么? _______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将NaHCO3溶液跟Al2(SO4)3溶液混合,相关反应的离子方程式是____________。
(2)有浓度均为0.2 mol·L-1的Na2CO3溶液与NaHCO3溶液,试回答下列问题:
①微粒种类:Na2CO3__________NaHCO3溶液(填“﹥”、“<”或“=”)。
②两溶液分别加入0.1 molNaOH固体,恢复到室温,Na2CO3溶液中的c(CO32-)____________(填“增大”、“减小”或“不变”);NaHCO3溶液中的c(HCO3-)_________(填“增大”、“减小”或“不变”)。
(3)常温下,甲为0.1 mol·L-1的HA溶液,pH﹥1;乙为0.1 mol·L-1的BOH溶液,且溶液中c(OH-):c(H+)=1012。请分别写出甲、乙两溶液中溶质的电离方程式:
甲__________________、乙_________________。
(4)相同条件下,对于浓度均为0.1 mol·L-1的NaCl溶液和CH3COONa溶液,溶液中的离子总数:NaCl溶液__________CH3COONa溶液(填“﹥”、“<”或“=”)。
(5)物质的量浓度相同的 ①氨水 ②氯化铵 ③碳酸氢铵 ④硫酸氢铵 ⑤硫酸铵五种溶液中c(NH4+)由大到小的顺序为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com