
【题目】图为某同学设计的原电池装置
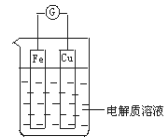
(1)当电解质溶液为稀硫酸时:
①Fe电极是_______(填“正”或“负”)极,其电极反应为_______
②Cu电极的电极反应为_________,该电极发生______反应(填“氧化”或“还原”)反应。原电池工作一段时间后,铁片的质量减少了2.8克,铜片表面产生气体____L(标准状况下),导线中通过_____mol电子。
(2)当电解质溶液为稀硝酸时:
①Fe电极是______极,其电极反应为________________,
②Cu电极是_____极,其电极反应为_________________,
【答案】负 Fe-2e-=Fe2+ 2H++2e-=H2↑ 还原 1.12L 0.1 负 Fe-2e-=Fe2+ 正 NO![]() +4H++3e-=NO↑+2H2O
+4H++3e-=NO↑+2H2O
【解析】
(1)①当电解质溶液为稀硫酸时电池总反应为Fe+H2SO4= H2↑+FeSO4,所以铁电极发生氧化反应为负极,电极反应式为Fe-2e-=Fe2+;
②铜电极上氢离子得电子生成氢气,电极反应式为2H++2e-=H2↑,发生还原反应;铁片减少2.8g,物质的量为![]() =0.05mol,根据电极反应式可知转移电子为0.1mol,生成氢气的物质的量为0.05mol,标况下的体积为0.05mol×22.4L/mol=1.12L;
=0.05mol,根据电极反应式可知转移电子为0.1mol,生成氢气的物质的量为0.05mol,标况下的体积为0.05mol×22.4L/mol=1.12L;
(2)①当电解质溶液为稀硝酸时,由于Fe比Cu活泼,所以电池总反应为3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O;所以Fe电极为负极,电极反应式为Fe-2e-=Fe2+;
②Cu电极上硝酸根得电子发生还原反应,所以Cu为正极,电极反应式为NO![]() +4H++3e-=NO↑+2H2O。
+4H++3e-=NO↑+2H2O。


科目:高中化学 来源: 题型:
【题目】在给定的条件下,下列选项所示的物质间转化均能一步实现的是( )
A.Fe![]() FeCl3(aq)
FeCl3(aq)![]() FeCl2(aq)
FeCl2(aq)
B.S![]() SO2
SO2![]() (NH4)2SO4(aq)
(NH4)2SO4(aq)
C.NaCl(熔融)![]() Na
Na![]() Na2O
Na2O
D.CuSO4(aq)![]() Cu(OH)2(s)
Cu(OH)2(s)![]() Cu2O(s)
Cu2O(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 水电离出的c(H+)·c(OH-)=10-22的溶液:K+、Na+、SO42-、S2O32-
B. 澄清透明溶液:Mg2+、Cu2+、Cl-、SO42-
C. 使酚酞变红色的溶液:NH4+、K+、AlO2-、SO32-
D. 含0.1 mol·L-1 KI的溶液:Fe3+、Na+、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下图:
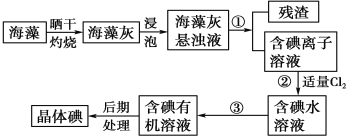
(1)实验室焙烧海带,需要下列仪器中的________(填序号)。
a 试管 b 烧杯 c 坩埚 d 泥三角 e 铁三脚架 f 酒精灯
(2)指出提取碘的过程中有关的实验操作名称:①__________,③________。
(3)提取碘的过程中,可选择的有机试剂是(_______)
A 甲苯、酒精 B 四氯化碳、苯
C 汽油、乙酸 D 汽油、甘油
(4)为使海藻灰中碘离子转化为碘的有机溶液,实验室有烧杯、玻璃棒、集气瓶、酒精灯、导管、圆底烧瓶、石棉网以及必要的夹持仪器、物品,尚缺少的玻璃仪器有__________、__________。
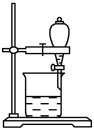
(5)小组用CCl4萃取碘水中的碘,在右图的分液漏斗中,下层液体呈__________色;
(6)从含碘的有机溶液中提取碘和回收有机溶剂,还须经过蒸馏,指出下面实验装置图中的错误之处:
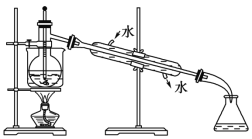
①____________________;
②_______________________________;
③____________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等.工业上用铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下:

(1)氧化炉中Al2O3、Cl2和C反应的化学方程式______.
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式______.
(3)为了测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,再洗涤、灼烧、冷却、称重、得其质量为0.32g。
①写出上述测定过程中涉及的离子方程式:______、__________。
②AlCl3产品的纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】BMO(Bi2MoO6)是种高效光催化剂,可用于光催化降解苯酚,原理如图所示。下列说法错误的是
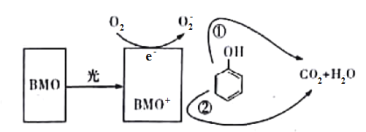
A.该过程的总反应为:C6H6O+ 7O2![]() 6CO2+3H2O
6CO2+3H2O
B.该过程中BMO+表现出较强的氧化性
C.①和②中被降解的苯酚的物质的量之比为1:3
D.光催化降解过程中,光能转化为化学能、热能等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(结构式如图所示)是常用的还原剂,由H·C·Brown和Schlesinger于1942年在芝加哥大学发现。其中X、Y、Z是原子序数依次减小的不同短周期主族元素,X与W、Z与W均能形成原子个数比为1:1和2:1的化合物,W原子的最外层电子数是电子层数的3倍。下列叙述正确的是
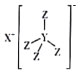
A.Z元素位于第三周期第Ⅶ A族
B.Y的最高价氧化物对应的水化物是一种一元弱酸
C.X和Z形成的化合物的水溶液呈酸性
D.化合物M不能与Z2W2反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知研究氮及其化合物的转化对于环境改善有重大意义。
I.已知N2(g) +O2(g)=2NO(g) △H=+180.4 kJ/mol,
4NH3(g)+5O2(g)=4NO(g)+6H2O(l) △H=![]() kJ/mol。
kJ/mol。
(1)用NH3消除NO污染的反应为:4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(l) △H=_______。则该反应自发进行的条件是______________(填“高温”或“低温”)。
5N2(g)+6H2O(l) △H=_______。则该反应自发进行的条件是______________(填“高温”或“低温”)。
(2)不同温度条件下,NH3与NO的物质的量之比分别为4:1、3:1、1:3,得到NO脱除率曲线如图所示。曲线a中NH3的起始浓度为4×10- 5mol/L,从A点到B点经过2秒,该时间段内NO的脱除速率为_______mg/(L·s),在AB所在的曲线上当温度高于900℃时NO脱除率明显降低的原因是_______________________________________________。
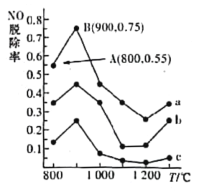
Ⅱ.用活性碳还原法也可以处理氮氧化合物,发生的反应为2CO(g)+ 2NO(g)![]() N2(g)+2CO2(g) △H=-746.8kJ/mol。
N2(g)+2CO2(g) △H=-746.8kJ/mol。
(3)在一恒容绝热的密闭容器中,能表示上述反应达到平衡状态的是_____________(填字母代号)。
A.单位时间内断裂1 mol N≡N键的同时生成2 mol C=O键
B.容器内的总压强保持不变
C.混合气体的密度保持不变
D.c(NO):c(N2):c(CO2)=2:1:2
E.混合气体的平均摩尔质量保持不变
(4)向一恒容密闭容器中充入3mol CO和2mol NO,测得气体的总压为10MPa,在一定温度下开始反应,10 min后达到平衡,测得NO的转化率为75%,该反应的平衡常数KP=____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅲ.用间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图所示,质子膜允许H+和H2O通过。
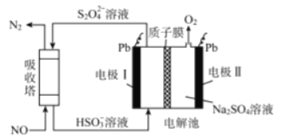
(5)写出吸收塔中的离子反应方程式_____________________________________,反应过程中若通过质子交换膜的H+为1 mol时,吸收塔中生成的气体在标准状况下的体积为_____ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A的产量是衡量一个国家石油化工生产水平的重要标志,以A为主要原料合成一种具有果香味的物质E的生产流程如下:
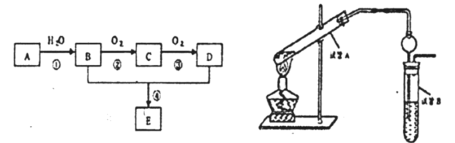
(1)有机物C的名称是_______________
(2)写出B→C的化学方程式________________
(3)请写出B+D→E的化学方程式________________
(4)试管A中加少许碎瓷片的目的是_______________
(5)试管B中试剂的作用是____________________
(6)右边试管接有一个球状物代替了长导管,其作用为______________
(7)从制备乙酸乙酯所得的混合物中分离提纯乙酸乙酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是_____________(填字母)

(8)酯化反应是一一可逆反应, 为提高乙醇的利用率,可采取的措施是_______________。(任写一种即可)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com