
【题目】CH4既是一种重要的能源,也是一种重要的化工原料.
(1)已知8.0g CH4完全燃烧生成液体水放出444.8kJ热量.则CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=kJmol﹣1
(2)以CH4为燃料可设计成结构简单、能量转化率高、对环境无污染的燃料电池,其工作原理图1所示,则通入a气体的电极名称为 , 通入b气体的电极反应式为 . (质子交换膜只允许H+通过)
(3)在一定温度和催化剂作用下,CH4与CO2可直接转化成乙酸,这是实现“减排”的一种研究方向.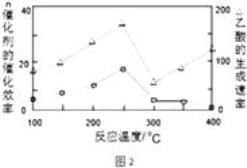
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图2所示,则该反应的最佳温度应控制在 左右.
②该反应催化剂的有效成分为偏铝酸亚铜(CuAlO2 , 难溶物).将CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,其离子方程式为 .
(4)CH4还原法是处理NOx气体的一种方法.已知一定条件下CH4与NOx反应转化为N2和CO2 , 若标准状况下8.96L CH4可处理22.4L NOx,则x值为 .
【答案】
(1)﹣889.6
(2)负极;O2+4e﹣+4H+=2H2O
(3)250℃;3 CuAlO2+16 H++NO3﹣=NO↑+3 Al3++3Cu2++8H2O
(4)1.6
【解析】解:(1)已知8.0g CH4完全燃烧生成液体水放出444.8kJ热量,则1mol即16g燃烧放出的热量为 ![]() ×444.8kJ=889.6kJ,反应放热,则故△H=﹣889.6kJ/mol;
×444.8kJ=889.6kJ,反应放热,则故△H=﹣889.6kJ/mol;
所以答案是:﹣889.6;
(2.)由图可知,通入气体a的一端发生氧化反应,故应通入甲烷,该极为负极,通入b为氧气,获得电子,酸性条件下结合氢离子生成水,正极电极反应式为:O2+4e﹣+4 H+=2H2O,
负极; O2+4e﹣+4H+=2H2O;
(3.)①从图象可知:250℃时乙酸反应速率最大、催化活性,故选择250℃;
所以答案是:250℃;②CuAlO2溶解在稀硝酸中生成两种盐并放出NO气体,生成的盐为硝酸铝、硝酸铜,反应还有水生成,反应离子方程式为:3 CuAlO2+16 H++NO3﹣=NO↑+3 Al3++3Cu2++8H2O;
所以答案是:3 CuAlO2+16 H++NO3﹣=NO↑+3 Al3++3Cu2++8H2O;
(4.)根据得失电子转移守恒,则:8.96L×[4﹣(﹣4)]=22.4L×2x,解得x=1.6;
所以答案是:1.6.


 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源: 题型:
【题目】氨水和盐酸是常见的化学试剂,可将氨气(NH3)、氯化氢气体分别溶于水制得. 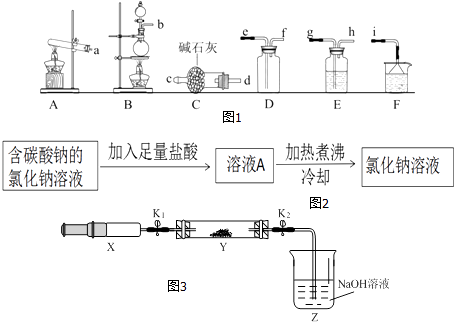
(1)氨气的发生装置可以选择如图1中的 , 反应的化学方程式为 .
(2)欲收集一瓶干燥的氨气,选择如图中的装置,其连接顺序为:发生装置→(按气流方向,用小写字母表示).
(3)小华为探究氨气溶于水是否发生化学反应,设计并完成如表实验(填写表中空白):
实验操作 | 实验现象及结论 |
将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
(4)小明将滴有酚酞的稀氨水加热,观察到溶液颜色变浅,原因可能是 .
(5)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化.为进一步研究,取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①>②,则稀盐酸经加热煮沸后浓度(填“增大”、“减小”或“不变”).为除去氯化钠溶液中的碳酸钠,小林设计了如图2方案:
你认为上述方案(填“合理”或“不合理”),请分析:(如合理,说明原因;如不合理,说明原因并设计改进方案).
(6)为研究氨气的还原性,小兰做了一下实验:
将(2)收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好).在一定温度如图3所示装置进行实验.
操作步骤 | 实验现象 | 解释原因 |
打开K1 , 推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中 | ②反应的化学方程式 |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
打开K2 | ③ | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组固体混合物分离操作正确的是
A. 碳酸钠和碳酸钙:溶解、过滤、蒸发(结晶)
B. 氯化钠和硫酸钠:溶解、过滤、蒸发(结晶)
C. 石灰石和氧化铁:溶解、过滤、蒸发(结晶)
D. 生石灰和碳酸钠:溶解、过滤、蒸发(结晶)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3,又名三氯化铁,是黑棕色结晶,主要用于金属蚀刻,污水处理。解答下列问题。
(1)按照物质的分类方法,FeCl3应属于_______________________。
①酸 ②氯化物 ③混合物 ④盐 ⑤化合物 ⑥电解质 ⑦易溶于水物质
A.②③④⑤⑥⑦ B.①④⑥⑦ C.②④⑤⑥⑦ D.④⑤⑥⑦
(2)0.1mol/LFeCl3溶液中c(Cl-)=_______mol/L。测得200mL某浓度FeCl3溶液中Cl-的质量为21.3g,则此溶液中c(Fe3+) =_______mol/L.
(3)将饱和FeCl3溶液逐滴加入沸水中,继续煮沸可制取氢氧化铁胶体,氢氧化铁胶体可处理污水,该反应的化学方程式为__________________;高铁酸钠Na2FeO4是一种新型水处理剂,用FeCl3制备的离子方程式如下,请完成该方程式的配平:___Fe3++_____Cl 2+_____OH-=_____FeO42-+_____Cl-+_____H2O
(4)FeCl3还可用于有机物的鉴别,已知芳香族化合物A、B、C的分子式均为C7H8O
A | B | C | |
加入氯化铁溶液 | 显紫色 | 无明显现象 | 无明显现象 |
加入钠 | 放出氢气 | 放出氢气 | 不反应 |
苯环上一氯代物的种数 | 2 | 3 | 3 |
则B的结构简式为____,A与浓溴水反应的方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种高分子化合物(VI)是目前市场上流行的墙面涂料之一,其合成路线如下(反应均在一定条件下进行):
回答下列问题:
(1)目前工业上生产乙烯主要是以为原料通过反应来实现.
(2)化合物III生成化合物IV的另外一种产物是 . (提示:该反应的逆反应原子利用率为100%)
(3)写出合成路线中从化合物IV到化合物VI的两步反应的化学方程式:、 .
(4)下列关于化合物III、IV和V的说法中,正确的是(填字母)
A.化合物III可以发生氧化反应
B.化合物III不可以与NaOH 溶液反应
C.化合物IV能与氢气发生加成反应
D.化合物III、IV和V均可与金属钠反应生成氢气
E.化合物IV和V均可以使溴的四氯化碳溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是2SO2(g) + O2(g) = 2SO3(g)反应过程中的能量变化, 已知1mol SO2(g)完全氧化为1mol SO3的ΔH= —99kJ·mol-1,请回答下列问题:
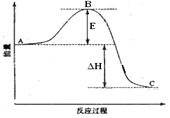
(1)图中A、C分别表的物质是__________________、________________,E的大小对该反应的焓变有无影响?___________(填“有”或“无”)(该反应通常用V2O5作催化剂,加V2O5会使图中B点降低。);
(2)图中△H = _____________kJ·mol-1;
(3)已知:S(s) + O2(g) = SO2(g) ΔH=-296 kJ·mol-1,计算由3 mol S(s)与氧气反应生成3 molSO3(g)的△H = ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于漂白粉的叙述正确的是
A. 漂白粉的有效成分是次氯酸钙和氯化钙 B. 漂白粉在空气中久置后会变质
C. 漂白粉是将氯气通入石灰水中制得 D. 漂白粉的主要成分是氯化钙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为原子序数递增的四种短周期元素,其中Y、Z为金属元素。X、Y、Z、W的最高价氧化物对应的水化物甲、乙、丙、丁之间存在如图所示反应关系(关系图中“—”相连的两种物质能发生反应)。下列判断正确的是
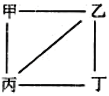
A. X是元素周期表中非金属性最强的元素 B. Z位于元素周期表第3周期IA族
C. 四种原子中,Y原子半径最小 D. W的简单阴离子可能促进水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的重要化合物如氨(NH3)、氮氧化物(NxOx)、肼(N2H4)、三氟化氮(NF3)等,在生产、生活中具有重要作用。
(1)①NH3催化氧化可制备硝酸。
4NH3(g)+5O2(g)===4NO(g)+6H2O(g) ΔH1=-907.28 kJ·mol-1
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ΔH2=-1269.02 kJ·mol-1
则4NH3(g)+6NO(g)===5N2(g)+6H2O(g) ΔH3=________________。
②NO被O2氧化为NO2。其他条件不变时,NO的转化率[α(NO)]与温度、压强的关系如下图所示。则p1________p2(填“>”“<”或“=”);温度高于800℃时,α(NO)几乎为0的原因是______________________________。

③在500℃温度时,2L密闭容器中充入2molNO和1molO2,达平衡时压强为P2MPa。则500℃时该反应的平衡常数Kp=_____________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
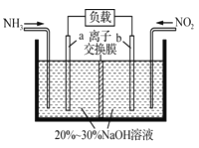
(2)利用反应NO2+NH3→N2+H2O(未配平)消除NO2的简易装置如下图所示。电极b的电极反应式为_________________,消耗标准状况下4.48LNH3时,被消除的NO2的物质的量为____________mol。
(3)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如下图所示。
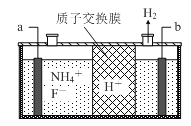
①a电极为电解池的_____________(填“阴”或“阳”)极,写出该电极的电极反应式:_____________;电解过程中还会生成少量氧化性极强的气体单质,该气体的分子式是_____________________。
②已知氨水电离常数Kb=1.8×10-5,氢氟酸电离常数Ka=3.5×10-4,则NH4F的电子式为_____________,0.1mol/LNH4F溶液中所有离子浓度由大到小的顺序为_____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com