
| 催化剂 |
| Cu或Ag |
| △ |
| 催化剂 |
| △ |
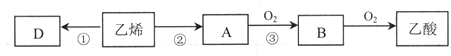
 ,生成聚乙烯,D为聚乙烯;
,生成聚乙烯,D为聚乙烯;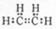 ,
,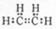 ;
;| 催化剂 |
| Cu或Ag |
| △ |
| Cu或Ag |
| △ |
 ,生成聚乙烯,
,生成聚乙烯, ;
;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、原来盐酸的物质的量浓度等于氨水的物质的量浓度 |
| B、所得溶液中c(NH4+)=c(Cl-) |
| C、所得溶液中c(NH4+)+c(H+)=c(Cl-) |
| D、所得溶液中c(NH4+)+c(NH3?H2O)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X分子中肯定有碳碳双键 |
| B、X分子中可能有三个羟基和一个-COOR官能团 |
| C、X分子中可能有三个羧基 |
| D、X分子中可能有一个羟基和二个羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
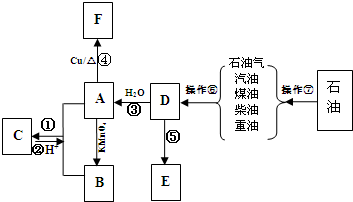
查看答案和解析>>
科目:高中化学 来源: 题型:
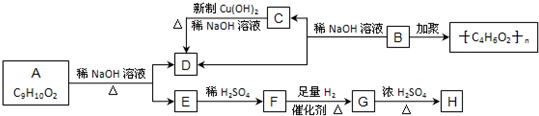
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com