
| A. | H2O | B. | KOH | C. | H2O2 | D. | CaO |
分析 只有氧元素形成的阴离子所构成的离子化合物中一定含有氧离子;一般非金属元素之间易形成共价键,金属元素与非金属元素之间易形成离子键,以此来分析.
解答 解:A.水是共价化合物,水中氧原子和氢原子之间只存在共价键,无氧离子,故A错误;
B.氢氧化钾是离子化合物,氢氧化钾中存在的化学键是由钾离子和氢氧根离子形成的离子键,无氧离子,故B错误.
C.H2O2是共价化合物,分子中氧原子和氢原子之间、氧原子和氧原子之间都只存在共价键,不存在氧离子,故C错误;
D.CaO是离子化合物,氧化钙中存在的化学键是由钙离子和氧离子形成的离子键,存在氧离子,故D正确.
故选D.
点评 本题考查了化学键的判断,难度不大,明确元素之间的成键原因是解答本题的关键.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 .
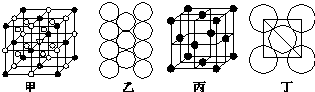
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | A的所有原子都在一个平面内 | B. | 反应①是加成反应 | ||
| C. | 反应②是消去反应 | D. | A的二取代产物只有1种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
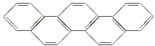 2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )
2016年夏季奥运会将在“足球王国”--巴西首都里约热内卢举行,如图酷似奥林匹克旗中的五环的一种有机物被称之为奥林匹克烃,下列说法正确的是( )| A. | 该有机物属于芳香族化合物,是苯的同系物 | |
| B. | 该有机物中只含非极性键 | |
| C. | 该有机物的一氯代物有11种 | |
| D. | 该有机物完全燃烧生成H2O的物质的量小于CO2的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | C2H4(SO2) | NaOH溶液 | 洗气 |
| B | C6H6(苯酚) | 浓Br2水 | 过滤 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H2(H2S) | CuSO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com