
【题目】将相同质量的两块铜片分别和浓硝酸、稀硝酸(两者均过量)反应,下列叙述正确的是( )
A.反应速率:两者相同
B.消耗HNO3的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
【答案】B
【解析】解:A、因为溶液浓度影响化学反应速率,浓度越大,反应速率越快,所以浓硝酸比稀硝酸反应速率快,故A错误;
B、铜与浓硝酸、稀硝酸反应方程式如下:
Cu+4HNO3(浓)=Cu(NO3)2+2NO2 ↑+2H2O
Cu+ ![]() HNO3=Cu(NO3)2+
HNO3=Cu(NO3)2+ ![]() NO↑+
NO↑+ ![]() H2O
H2O
根据方程式可知,浓硝酸消耗的物质的量多,故B正确;
C、根据B知,铜与浓硝酸反应生成二氧化氮,与稀硝酸反应生成一氧化氮,二氧化氮是红棕色气体,一氧化氮是无色气体,故C错误;
D、根据铜与转移电子的关系知,
Cu | + | 4HNO3(浓) | = | Cu(NO3)2 | + | 2NO2 ↑ | + | 2H2O | 转移电子 |
1mol | 2mol |
Cu | + |
| = | Cu(NO3)2 | + |
| + |
| 转移电子 |
1mol | 2mol |
根据方程式知,相同质量的铜与过量浓、稀硝酸反应转移电子数相等,故D错误.
故选B.


 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】 下列叙述正确的是
A.氧化还原反应的本质是化合价发生变化
B.有单质产生的分解反应一定是氧化还原反应
C.氧化剂在同一反应中既可以是反应物,也可以是生成物
D.还原剂在反应中发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面关于硅的叙述中,正确的是( )
A.粗硅制备单晶硅不涉及氧化还原反应
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X、Y与稀硫酸构成原电池时,Y为负极。X、Y、Z三种金属的活动性顺序为
A. Y>X>ZB. X>Z>YC. Y>Z>XD. X>Y>Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律分析下面的推断,其中不正确的是
A. Na的原子失去电子能力比Mg强
B. HBr比HCl稳定
C. Ca(OH)2 的碱性比 Mg(OH)2 的碱性强
D. H2SO4 比H3PO4 酸性强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列各溶液中,离子一定能大量共存的是( )
A.强碱性溶液中:K+、Al3+、Cl-、SO42-
B.含有0.1 molL-1 Fe3+的溶液中:K+、Mg2+、I-、NO3-
C.含有0.1 molL-1 Ca2+的溶液中:Na+、K+、CO32-、Cl-
D.室温下,pH=1的溶液中:Na+、Fe3+、NO3-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组欲对铝镁合金进行研究,测定其中镁的质量分数,他们利用盐酸、氢氧化钠溶液设计了三种不同的实验方案:
方案一:铝镁合金 ![]() 测定生成气体的体积
测定生成气体的体积
方案二:铝镁合金 ![]() 测定生成气体的体积
测定生成气体的体积
方案三:铝镁合金 ![]() 溶液
溶液 ![]()
![]() 称量灼烧产物的质量.
称量灼烧产物的质量.
(1)写出方案一中发生反应的离子方程式 .
(2)实验小组根据方案=设计了两个实验装置,如下圈(图中的铁架台已省略). 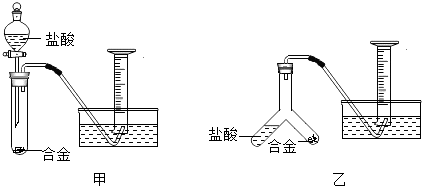
你认为选择(选填甲或乙)装置进行实验更合理,误差更小.
(3)用方案三进行实验时,除了称量灼烧产物质量外,还需称量的是 .
(4)拓展研究:在向铝镁合金溶于盐酸后的溶液中加入过量NaOH溶液时,生成沉淀的质量与加入NaOH溶液体积的关系可用数轴关系表示: 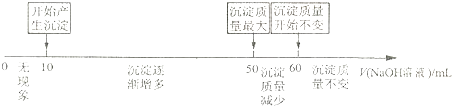
请你判断,根据如图数轴申的数据能否求出合金中镁的质量分数?(选填“能”或“不能”)
下列①②两题选一题作答.
①若不能求出合金中镁的质量分数,请说明理由.
②若能求出合金中镁的质量分数,则镁的质量分数为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com