
【题目】X、Y、Z都是金属,把X浸入Z的硝酸盐溶液中,X的表面有Z析出,X、Y与稀硫酸构成原电池时,Y为负极。X、Y、Z三种金属的活动性顺序为
A. Y>X>ZB. X>Z>YC. Y>Z>XD. X>Y>Z
科目:高中化学 来源: 题型:
【题目】温度为T℃时,向2.0L恒容密闭容器中充入1.0molPCl5 , 反应PCl5(g) PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11molL﹣1 , 则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2 , 达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl5、2.0molCl2 , 达到平衡时,PCl5的转化率大于20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:A(g)+xB(g)2C(g).各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以如表和如图表示: 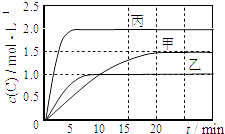
容器 | 甲 | 乙 | 丙 |
容积 | 0.5L | 0.5L | 1.0L |
温度/℃ | T1 | T2 | T2 |
反应物 | 1.5molA | 1.5molA | 6.0molA |
下列说法正确的是( )
A.x=1
B.10min内乙容器中反应的平均速率v(B)=0.025molL﹣1min﹣1
C.由图可知:T1<T2 , 且该反应为吸热反应
D.T1℃,起始时甲容器中充入0.5molA,1.5molB,平衡时A的转化率为75%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“无论从经济的发展还是人类的进步而言,合成氨的发明都是本世纪科学领域中最辉煌的成就之一.”图1是与NH3相关的工业过程示意图. 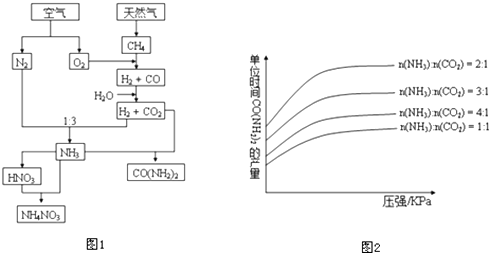
已知CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=﹣890kJmol﹣1
2CO(g)+O2(g)═2CO2(g)△H=﹣566.0kJmol﹣1
2H2(g)+O2(g)═2H2O(g)△H=﹣571.6kJmol﹣1
(1)请写出CH4(g)与O2(g)反应生成CO(g)和H2(g)的热化学反应方程式 .
(2)在生产过程中,会涉及H2和CO2的分离.你认为可取的方法是(填序号).
a.在加压条件下用水吸收CO2 b.用NaOH溶液吸收CO2 c.加压,使CO2液化
(3)合成尿素的反应是分作两步进行的:
①CO2(g)+2NH3(g)═H2NCOONH4(aq) (氨基甲酸铵)△H=﹣159.47kJmol﹣1
②H2NCOONH4(aq)═CO(NH2)2(aq)+H2O(l)△H=﹢28.49kJmol﹣1
在生产条件下,单位时间内获得尿素的产量与压强和n(NH3):n(CO2)的关系如图2所示.生产过程中n(NH3):n(CO2)的最佳配比为 , 而实际生产条件下,往往使n(NH3):n(CO2)≥3,这是因为、 . 在得到的尿素溶液中会含有少量的氨基甲酸铵,除去这种杂质最简便的方法是 .
(4)将氨分为两部分,一部分经逐级氧化吸收转化为硝酸,另一部分又与HNO3反应生成NH4NO3 . 若HNO3与NH3的反应是完全的,有标准状况下50LNH3经上述反应过程生成84g NH4NO3 . 则NH3逐级转化为HNO3的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O的说法正确的是( )
A. Cu是氧化剂
B. 该反应电子转移总数为4e—
C. 硝酸在反应中只体现氧化性
D. NO是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将相同质量的两块铜片分别和浓硝酸、稀硝酸(两者均过量)反应,下列叙述正确的是( )
A.反应速率:两者相同
B.消耗HNO3的物质的量:前者多,后者少
C.反应生成气体的颜色:前者浅,后者深
D.反应中转移的电子总数:前者多,后者少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列由于物质的漂白性而导致溶液褪色的是( )
①将过氧化钠投入水中,然后加入几滴酚酞溶液,溶液先变红后褪色
②将活性炭放入红墨水中,溶液褪色
③向品红溶液中滴加氯水,红色褪去
④向酸性高锰酸钾溶液中通入二氧化硫气体,溶液紫色褪去
A.①③
B.①②③
C.①②③④
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种可再生能源,具有广泛的开发和应用前景.请回答下列与甲醇有关的问题.
(1)甲醇分子是分子(填“极性”或“非极性”).
(2)工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)CH3OH(g)△H=﹣86.6KJ/mol,在T℃时,往一个体积固定为1L的密闭容器中加入1mol CO和2mol H2 , 反应达到平衡时,容器内的压强是开始时的3/5.
①达到平衡时,CO的转化率为
②下列选项能判断该反应达到平衡状态的依据的有
A.2v(H2)=v(CH3OH) B.CO的消耗速率等于CH3OH的生成速率
C.容器内的压强保持不变 D.混合气体的密度保持不变
E.混合气体的平均相对分子质量不随时间而变化
(3)已知在常温常压下:
①2CH3OH(1)+3O2(g)=2CO2(g)+4H2O(g)△H=﹣akJmol﹣1
②2CO(g)+O2(g)=2CO2(g)△H=﹣bklmol﹣1
③H2O(g)=H2O(1)△H=﹣ckJmol﹣1
则CH3OH(1)+O2(g)═CO(g)+2H2O(1)△H=kJmol﹣1
(4)由甲醇、氧气和NaOH溶液构成的新型手机电池,可使手机连续使用一个月才充一次电.
①该电池负极的电极反应式为 .
②若以该电池为电源,用石墨做电极电解200mL含有如下离子的溶液.
离子 | Cu2+ | H+ | Cl﹣ | SO42﹣ |
c/molL﹣1 | 0.5 | 2 | 2 | 0.5 |
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存在的溶解现象)阳极上收集到氧气的质量为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com