
����Ŀ�������۴Ӿ��õķ�չ��������Ľ������ԣ��ϳɰ��ķ������DZ����Ϳ�ѧ��������Ի͵ijɾ�֮һ����ͼ1����NH3��صĹ�ҵ����ʾ��ͼ�� 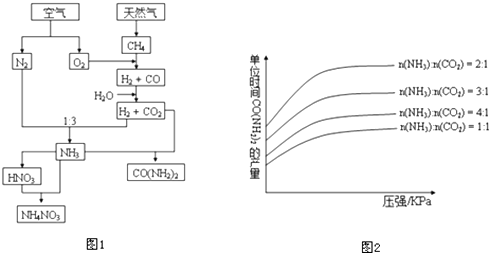
��֪CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=��890kJmol��1
2CO��g��+O2��g���T2CO2��g����H=��566.0kJmol��1
2H2��g��+O2��g���T2H2O��g����H=��571.6kJmol��1
��1����д��CH4��g����O2��g����Ӧ����CO��g����H2��g�����Ȼ�ѧ��Ӧ����ʽ ��
��2�������������У����漰H2��CO2�ķ��룮����Ϊ��ȡ�ķ�����������ţ���
a���ڼ�ѹ��������ˮ����CO2 b����NaOH��Һ����CO2 c����ѹ��ʹCO2Һ��
��3���ϳ����صķ�Ӧ�Ƿ����������еģ�
��CO2��g��+2NH3��g���TH2NCOONH4��aq�� ����������泥���H=��159.47kJmol��1
��H2NCOONH4��aq���TCO��NH2��2��aq��+H2O��l����H=��28.49kJmol��1
�����������£���λʱ���ڻ�����صIJ�����ѹǿ��n��NH3����n��CO2���Ĺ�ϵ��ͼ2��ʾ������������n��NH3����n��CO2����������Ϊ �� ��ʵ�����������£�����ʹn��NH3����n��CO2����3��������Ϊ�� �� �ڵõ���������Һ�лẬ�������İ�������泥���ȥ������������ķ����� ��
��4��������Ϊ�����֣�һ���־�����������ת��Ϊ���ᣬ��һ��������HNO3��Ӧ����NH4NO3 �� ��HNO3��NH3�ķ�Ӧ����ȫ�ģ��б�״����50LNH3��������Ӧ��������84g NH4NO3 �� ��NH3��ת��ΪHNO3��ת����Ϊ ��
���𰸡�
��1��2CH4��g��+O2��g���T2CO��g��+4H2��g����H=��70.8kJ/mol
��2��c
��3��2��1�����������CO2��ת���ʣ���ΪNH3��������ˮ�����ڷ��롢�������ã�����
��4��89%
���������⣺��1.����CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=��890kJ/mol
��2CO��g��+O2��g���T2CO2��g����H=��566.0kJ/mol
��2H2��g��+O2��g���T2H2O��g����H=��571.6kJ/mol��
���ݸ�˹���ɣ�CH4��g����O2��g����Ӧ����CO��g����H2��g�����Ȼ�ѧ��Ӧ����ʽΪ���١�2���ک��ۡ�2
��2CH4��g��+O2��g���T2CO��g��+4H2��g����H=��70.8kJ/mol��
���Դ��ǣ�2CH4��g��+O2��g���T2CO��g��+4H2��g����H=��70.8kJ/mol��
��2.��a����Ϊ������̼��ˮ�е��ܽ��ԱȽ�С�����Բ�����ˮ���գ��ʴ���
b����NaOH��Һ����CO2 �� �������µ����ʣ��ʴ���
c����ѹ��ʹCO2Һ�������������������ȷ��
���Դ��ǣ�c��
��3.������ͼ���������������n��NH3����n��CO2����������Ϊ2��1����Ϊ������̼���ܽ��ԱȽ�С������ʵ����������Ҫ���������������������CO2��ת���ʣ���ΪCO2��g��+2NH3��g��H2NCOONH4��aq����H=��159.47kJ/mol�����Գ�ȥ������������ķ����Ǽ������£�ʹƽ�������ƶ���
���Դ��ǣ�2��1�����������CO2��ת���ʣ���ΪNH3��������ˮ�����ڷ��롢�������ã����ȣ�
��4.�������б�״����50LNH3�� ![]() =2.23mol����������Ӧ��������84g NH4NO3��
=2.23mol����������Ӧ��������84g NH4NO3�� ![]() =1.05mol��������������淋İ����������1.05mol��������������ʣ��İ������ɵģ�����2.23mol��1.05mol=1.18mol��������1.05mol�����ᣬ���ݵ��غ���NH3��HNO3 �� ����NH3ת��ΪHNO3��ת����
=1.05mol��������������淋İ����������1.05mol��������������ʣ��İ������ɵģ�����2.23mol��1.05mol=1.18mol��������1.05mol�����ᣬ���ݵ��غ���NH3��HNO3 �� ����NH3ת��ΪHNO3��ת���� ![]() ��100%=89%��
��100%=89%��
���Դ��ǣ�89%��


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣���ش��й����⣺
��1���ݺ͢��Ԫ�ط��ŷֱ�������
��2����������õĽ����� �� �ǽ�������ǿ��Ԫ����(��Ԫ�ط��ţ���ͬ)��
��3���������γ��������������Ԫ���� �� �ֱ�д����Ԫ�ص�����������͢������������ˮ���ﷴӦ�Ļ�ѧ����ʽ����
��4�������һ��ʵ�鷽�����ȽϢߺ͢�ĵ��������Ե�ǿ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ڹ�������У���ȷ���ǣ� ��
A.�ֹ��Ʊ������費�漰������ԭ��Ӧ
B.���ǹ��ɿ������ʯ����ҪԪ�أ����ڵؿ��еĺ��������е�Ԫ���оӵ�һλ
C.��Ļ�ѧ���ʲ����ã�����Ȼ���п���������̬����
D.���ڵ��ӹ�ҵ�У�����Ҫ�İ뵼�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ�����ʾ��ȷ���ǣ� ��
A.NaH����ˮ��Ӧ�ķ���ʽ��NaH+D2O=NaOH+D2��
B.���������ĵ���ʽ�� ![]()
C.����״̬���������Ƶĵ��뷽��ʽ��NaHSO4�����ڣ�=Na++HSO4��
D.�ǻ����ᣨHOCH2COOH��������� ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z���ǽ�������X����Z����������Һ�У�X�ı�����Z������X��Y��ϡ���ṹ��ԭ���ʱ��YΪ������X��Y��Z���ֽ����Ļ��˳��Ϊ
A. Y>X>ZB. X>Z>YC. Y>Z>XD. X>Y>Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�����ڱ���Ԫ�������ɷ���������ƶϣ���������ȷ����
A. Na��ԭ��ʧȥ����������Mgǿ
B. HBr��HCl�ȶ�
C. Ca��OH��2 �ļ��Ա� Mg��OH��2 �ļ���ǿ
D. H2SO4 ��H3PO4 ����ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ��ƾ���,����������ȷ����(����)
A.�����������ܶѻ���һ������
B.58.5g�Ȼ��ƾ�����Լ��6.02��1023��NaCl����
C.���Ȼ�菉���ṹ��ͬ
D.ÿ��Na+��6��Cl-��Ϊ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com