
����ѧ��ѡ��3�� ���ʽṹ�����ʡ��ѡ�������������ͭ�Ƚ������仯�����ڹ�ҵ������Ҫ��;��
��1�������Ͻ�����ϵ����Ͻ�Ĵ������úϽ���з����¶ȵ͡��۸����е��ŵ㡣
��Ti�Ļ�̬ԭ�Ӽ۵����Ų�ʽΪ________________��
��Fe�Ļ�̬ԭ�ӹ���________�ֲ�ͬ�ܼ��ĵ��ӡ�
��2���Ʊ�CrO2Cl2�ķ�ӦΪK2Cr2O7��3CCl4===2KCl��2CrO2Cl2��3COCl2����
��������ѧ����ʽ�зǽ���Ԫ�ص縺���ɴ�С��˳����______________(��Ԫ�ط��ű�ʾ)��
��COCl2����������ԭ�Ӿ�����8���ӹ��ͣ�COCl2�����ЦҼ��ͦм��ĸ�����Ϊ________������ԭ�ӵ��ӻ���ʽΪ________��
��3��NiO��FeO�ľ���ṹ�����Ȼ��Ƶľ���ṹ��ͬ������Ni2����Fe2�������Ӱ뾶�ֱ�Ϊ6.9��10��2 nm��7.8��10��2 nm�����۵㣺NiO________(���������<������)FeO��
��4��Ni��La�ĺϽ���Ŀǰʹ�ù㷺�Ĵ�����ϣ����д����������������͵��µ��ص㣬���ձ����й���ʵ���˲�ҵ����
�úϽ�ľ����ṹ��ͼ��ʾ��
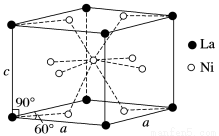
�ٸþ���Ļ�ѧʽΪ________________��
����֪�þ�����Ħ������ΪM g��mol��1���ܶ�Ϊd g��cm��3����NAΪ�����ӵ�������ֵ����þ����������________ cm3(�ú�M��d��NA�Ĵ���ʽ��ʾ)��
�۸þ�����ڲ����п�϶����ÿ�������Ŀ�϶�д���6����ԭ�ӱȽ��ȶ�����֪��a��511 pm��c��397 pm����״�����������ܶ�Ϊ8.98��10��5 g��cm��3������������ ������������ǰ��������仯����ô�����ϵĴ�������Ϊ_______��
������������ǰ��������仯����ô�����ϵĴ�������Ϊ_______��
 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭������һ�и�һ�µڶ��ζο���ѧ�Ծ��������棩 ���ͣ������
��Ҫ����գ�
��1�����켼����ʹ�õ�����ȼ�ϵ�ؾ��и��ܡ���㡢����Ⱦ�������ŵ㣬��ʽ����ȼ�ϵ���еĵ�����Ǽ��������Ӧ��ʾΪ��O2+2H2O+4e- 4OH-�����为����Ӧ�ɱ�ʾΪ__________________��
4OH-�����为����Ӧ�ɱ�ʾΪ__________________��
��2����һ�������£�RO3n-��I-������Ӧ�����ӷ���ʽ���£� RO3n-+6I-+6H+=R-+3I2+3H2O
��RԪ�ص�ԭ������������ ����
��3��Na2SX�ڼ�����Һ�пɱ�NaClO����ΪNa2SO4����NaClO����ԭΪNaCl������Ӧ��Na2Sx��NaClO�����ʵ���֮��Ϊ1:16����xֵ��
��4��CH4��H2O��g��ͨ��۽�̫���ܷ�Ӧ���У�������Ӧ��CH4��g��+H2O��g��?CO��g��+3H2��g�����������ʵ�����CH4��H2O��g������2L�����ܱշ�Ӧ���У�ij�¶��·�Ӧ�ﵽƽ��ʱ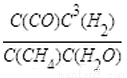 =27����ʱ���n��CO��=0.2mol����ƽ��ʱCH4��ת����Ϊ ����������������λ��Ч���֣���
=27����ʱ���n��CO��=0.2mol����ƽ��ʱCH4��ת����Ϊ ����������������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ�������һ��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ҩ�ﰢ˾ƥ�ֿ���ˮ�����Ƶã����ǵĽṹ��ͼ��ʾ���й�˵����ȷ����
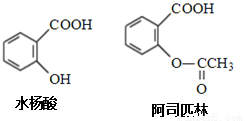
A�����ð�˾ƥ�֣��������ˮ�������Ӧʱ���ɾ���ע��NaHCO3��Һ
B����˾ƥ�ֵķ���ʽΪC9H10O4
C��1 mol��˾ƥ����������2 mol NaOH
D��ˮ������Է���ȡ�����ӳɡ��������Ӿ۷�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʦ���и������һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
����ѧ�Cѡ��2����ѧ�뼼������ҵ����ƽ�VOSO4�е�K2S O4��SiO2���ʳ�ȥ�����յõ�V2O5���������£�
O4��SiO2���ʳ�ȥ�����յõ�V2O5���������£�

��ش��������⣺
��1����������÷����ijɷ��� ��д��ѧʽ��������I������ ��
��2������ڡ��۵ı仯���̿ɼ�Ϊ����ʽR��ʾVO2+��HA��ʾ�л���ȡ������
R2(SO4)n (ˮ��)��2nHA���л��㣩 2RAn���л��㣩��nH2SO4 (ˮ��)
2RAn���л��㣩��nH2SO4 (ˮ��)
������ȡʱ��������������ԭ���� ��
����X�Լ�Ϊ ��
��3���ܵ����ӷ���ʽΪ ��
��4��25��ʱ��ȡ����������������õ��������ʺ���ҺpH֮���ϵ���±���
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
��������% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
����ϱ�����ʵ�������У����м��백ˮ��������Һ�����pHΪ ��
����������Ϊ93.1%ʱ������Fe(OH)3����������Һ��c(Fe3+)�� ��
����֪��25��ʱ��Ksp[Fe(OH)3]��2.6��10��39��
��5���ù��������У�����ѭ�����õ������� �� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʦ���и������һ�����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�˵����ȷ����
A��2,2-����������2,4-���������һ�ȴ���������ͬ
B�����顢������������Һ������ʹ���Ը��������Һ��ɫ
C�������ܶȱ�ˮС�����ɱ���Ӧ�Ƶõ��屽������������������ܶȶ���ˮ��
D�����������ڼ��������µ�ˮ�ⷴӦ��Ϊ������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ���������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
25��ʱ��0.1 mol Na2CO3�����������õ�һ�����Ϊ1 L����Һ����Һ�в�������pH �Ĺ�ϵ����ͼ��ʾ�������й���Һ������Ũ�ȹ�ϵ������ȷ����( ��

A. W����ʾ����Һ�У�c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(Cl-)
B. pH=4����Һ�У�c(H2CO3)+c(HCO32-)+c(CO32-)<0.1 mol��L-1
C. pH=8����Һ�У�c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-)
D. pH=11����Һ�У�c(Na+)��c(Cl-)��c(CO32-)��c(HCO32- )��c(H2CO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ��ƶ���
���������ű������ڡ��ƹ������м�������ܻ����������ܻ��������������ܼ�����ѧ�����ڱ��������������������ѧʽ��C16H22O4 , ���ڹ�ҵ����;�dz��㷺������������������Σ�����������ܻ���������ܶ࣬����һ�֡��ܻ��������Ʊ�������ͼ��

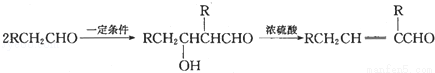
��֪��
��ش��������}��
��1������ˮ�ⷴӦ���䷴Ӧ����Ϊ�� ��
��2��д����ͼ��Ӧ�ķ�Ӧ���ͣ��� ���� ���� ��
��3��д�����з���ʽ���� ���� ���� ��
��4��д��D�����������Һ�����������ͬ���칹���� �֣�д������һ�ֺ˴Ź���������3���壬����ԭ����Ϊ6��1��1�Ľṹʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����±��е��ĸ��Ȼ�ѧ����ʽ���ж������ͱ����ȼ���ȷֱ���
���϶�һ�š�������ȼ�� | Һ��(H2) | ��2H2(g)+O2(g) ��2H2(l)+O2(l) |
�������˻ᡰ���ơ����ȼ�� | ���� (C3H8) | ��C3H8(l)+5O2(g) ��C3H8(g)+5O2(g) |
A.571.6 kJ��mol-1,2 221.5 kJ��mol-1
B.241.3 kJ��mol-1,2 013.8 kJ��mol-1
C.285.8 kJ��mol-1,2 013.8 kJ��mol-1
D.285.8 kJ��mol-1,2 221.5 kJ��mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������и�һ6��ѧҵ���л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ͬλ�أ�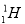 ��
��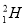 ��
��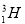 ������֮����ڲ������
������֮����ڲ������
A�������� B�������� C�������� D��ԭ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com