
【题目】铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:

(1)操作Ⅰ的名称是__________________________。
(2)检验FeCO3沉淀是否洗净的实验方法是__________________________。
(3)在空气中煅烧FeCO3的化学方程式是____________________________。
(4)称取3.0 g 产品,用稀硫酸溶解,逐滴加入0.10 mol·L-1 KMnO4溶液20.00 mL,二者恰好反应完全。若此产品中只含有FeO、Fe2O3,求算产品中Fe2O3的质量分数,写出计算过程。(已知:10FeSO4+2KMnO4+8H2SO4=5Fe2(SO4)3+2MnSO4+K2SO4+8H2O)________________
【答案】过滤 取最后一次洗涤液少量于试管中,加入盐酸无现象,再加入BaCl2溶液,若无白色沉淀生成,则洗净 4FeCO3+O2 ![]() 2Fe2O3+4CO2 76%
2Fe2O3+4CO2 76%
【解析】
废铁屑与稀硫酸反应生成硫酸亚铁和氢气,过滤除去不溶于酸的杂质,得到硫酸亚铁溶液,向硫酸亚铁溶液中加入碳酸氢铵,反应生成硫酸铵、碳酸亚铁、二氧化碳和水,过滤得到碳酸亚铁固体,用冰水洗涤除去碳酸亚铁固体表面的可溶性杂质后,煅烧FeCO3固体,FeCO3与空气中氧气反应生成氧化铁和二氧化碳。
(1)操作Ⅰ是把沉淀和废液分离的操作,操作Ⅰ的名称是过滤,故答案为:过滤;
(2)固体表面可能带有SO42-,检验FeCO3沉淀是否洗净,可以检验洗涤液中是否含有SO42-,取最后一次洗涤液少量于试管中,加入盐酸无现象,再加入BaCl2溶液,若无白色沉淀生成,则洗净,故答案为:取最后一次洗涤液少量于试管中,加入盐酸无现象,再加入BaCl2溶液,若无白色沉淀生成,则洗净;
(3)在空气中煅烧FeCO3,FeCO3被氧气氧化为Fe2O3,煅烧的方程式是4FeCO3+O2 ![]() 2Fe2O3+4CO2,故答案为:4FeCO3+O2
2Fe2O3+4CO2,故答案为:4FeCO3+O2 ![]() 2Fe2O3+4CO2;
2Fe2O3+4CO2;
(4)设样品含FeO的质量是xg,根据方程式可得关系式:
5FeO ~ KMnO4
5×72g 1mol
xg 0.10 mol·L-1×0.02L
解![]() 可得x=0.72g,产品中Fe2O3的质量分数
可得x=0.72g,产品中Fe2O3的质量分数![]() 76%,故答案为:76%。
76%,故答案为:76%。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 胶体与溶液的本质区别在于是否可以发生丁达尔现象
B. 在常温下铁遇浓硫酸会钝化,所以可以用铁制容器来装运浓硫酸
C. 氯气具有漂白性,可以使湿润的有色布条褪色
D. 二氧化碳通入足量澄清石灰水中,没有白色沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】采用乙烯与甲苯为主要原料,按下列路线可合成有机物 E、F:
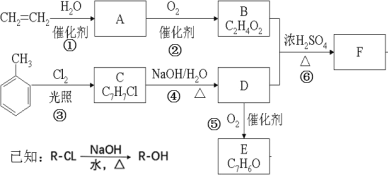
请回答:
(1)B 中官能团的名称是_________,反应⑥的反应类型是__________。
(2)D→E 的 化 学 方 程 式_________________________________。
(3)F 的 结 构 简 式___________________________。
(4)下列有关说法不正确的是_________。
A.E 能与新制的 Cu(OH)2 悬浊液发生反应,而 B 不能与新制的 Cu(OH)2 悬浊液发生反应
B.F 在碱性条件下可发生皂化反应
C. ![]() 不能使酸性 KMnO4 溶液褪色
不能使酸性 KMnO4 溶液褪色
D. 1mol E 和足量 H2 反应,最多消耗 4mol H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子交换法净化水过程如图所示。下列说法中错误的是

A. 经过阳离子交换树脂后,水中阳离子的总数不变
B. 水中的![]() 、
、![]() 、Cl通过阴离子树脂后被除去
、Cl通过阴离子树脂后被除去
C. 通过净化处理后,水的导电性降低
D. 阴离子树脂填充段存在反应H++OH![]() H2O
H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中几种常见物质的转化关系如下:

将D溶液滴入沸水中可得到以F为分散质的红褐色胶体。请回答下列问题:
(1)红褐色胶体中F粒子直径大小的范围:___________________________________。
(2)写出B的化学式:B________。
(3)①H2O2分子的电子式:__________________________________。
②写出C的酸性溶液与双氧水反应的离子方程式:_________________________。
(4)写出鉴定E中阳离子的实验方法和现象:____________________________。
(5)在C溶液中加入与C等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于置换反应X+M→Y+N(未配平,反应条件略去),其中X、Y为单质,M、N为化合物,下列说法中错误的是( )
A. 若M为H2O,则Y可能为O2
B. 若M为NH3,则X可能为Cl2
C. 若Y为Fe,则X一定是H2
D. 若Y为C,则N可能为MgO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度条件下, 甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g)![]() xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是
A. 若平衡时,甲、乙两容器中A的物质的量不相等,则x=2
B. 平衡时,甲、乙两容器中A、B的物质的量之比不相等
C. 平衡时甲中A的体积分数为40%
D. 若平衡时两容器中的压强不相等,则两容器中压强之比为8∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是
A. NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s) ![]() NaOH(aq)
NaOH(aq)
B. Al(s)![]() NaAlO2(aq)
NaAlO2(aq)![]() Al(OH)3(s)
Al(OH)3(s)
C. AgNO3(aq)![]() [Ag(NH3)2]+(aq)
[Ag(NH3)2]+(aq)![]() Ag(s)
Ag(s)
D. Fe2O3(s)![]() Fe(s)
Fe(s)![]() FeCl3(aq)
FeCl3(aq)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代半导体材料氮化镓(GaN)适合于制作高温、高频、抗辐射及大功率器件,通常称为高温半导体材料。回答下列问题:
(1)基态Ga原子价层电子的轨道表达式为_______,第一电离能介于N和B之间的第二周期元素有_______种。
(2)HCN分子中σ键与π键的数目之比为_______,其中σ键的对称方式为______。与CN-互为等电子体的分子为__________。
(3)NaN3是汽车安全气囊中的主要化学成分,其中阴离子中心原子的杂化轨道类型为_________,NF3的空间构型为_________。
(4)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,熔点如表所示,分析其变化原因_____________。
GaN | GaP | GaAs | |
熔点 | 1700℃ | 1480℃ | 1238℃ |
(5)GaN晶胞结构如图所示:晶胞中Ga原子采用六方最密堆积方式,每个Ga原子周围距离最近的Ga原子数目为_________;


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com