
如图表示常见元素单质及化合物相应关系,某些生成物已略去。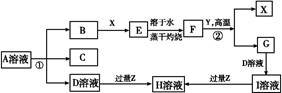
已知:反应①为氯碱工业的基础反应;X、Y为常见金属,Z为形成酸雨的主要成分。请回答下列问题:
(1)D的电子式 ;H为 (填化学式)。
(2)完成下列方程式:
①空气中含量最高的气体与C反应的化学反应方程式 ;
②反应②的化学反应方程式 ;
③足量B通入H溶液的离子反应方程式 。
科目:高中化学 来源: 题型:单选题
已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的最高价氧化物是耐火材料;H为气体单质,D为无色气体,在空气中会出现红棕色。各物质的转化关系如下图(部分反应产物已略去)。
请回答下列问题:
(1)X的化学式为 。
(2)在反应①②③④中属于置换反应的是 (填序号)。
(3)反应③的化学方程式为_________________________________。
(4)X溶液与F反应的总化学方程式为 。
(5)检验滤液A中金属离子的方法是 。
(6)若向100 mL盐X的溶液中加入10 g过量金属单质M的粉末,充分搅拌后,过滤,烘干得10.16g固体。则滤液A中溶质的物质的量浓度为_________。(假设溶液体积不变)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(13分).巳知 A、B、D为中学常见的单质,甲、乙、丙、丁、戊为短周期元素组成的化合物。其中,丙是一种能使湿润的红色石蕊试纸变蓝的无色气体;丁是一种高能燃料,其组成元素与丙相同,1 mol 丁分子中不同原子的数目比为1 :2,且含有18 mol电子;戊是一种难溶于水的白色胶状物质,既能与强酸反应,也能与强碱反应,具有净水作用。各物质间的转化关系如下图所示(某些条件巳略去)。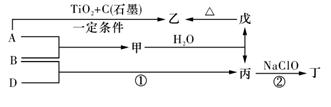
请回答:(1)单质B的组成元素在周期表中的位置是_________。
(2)戊的化学式为________。戊与强碱反应的离子方程式:________________
(3)丙中所包含的化学键类型有________ (填字母序号)。
a.离子键 b.极性共价键 c.非极性共价键
(4)反应①的化学方程式为________________________。
(5)反应②中,0.5mol NaClO参加反应时,转移1 mol电子,其化学方程式为_________
(6)—定条件下,A与TiO2、C(石墨)反应只生成乙和碳化钛(TiC),二者均为某些高温结构陶瓷的主要成分。巳知,该反应生成1 mol乙时放出536 kJ热量,其热化学方程式为_______________________
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A~H均为短周期元素,A~F在元素周期表中的相对位置如图1所示,G与其它七种元素
| 图1 | |||
| A | B | C | |
| D | | E | F |
| 图2 | |||
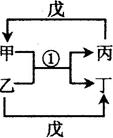 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
在下图转化关系中,固体甲的焰色反应呈黄色,M为常见的液体物质,I为一常见金属,酸G是重要的化工产品和化工原料;固体H能够溶解在A溶液和酸G中,且H为良好的耐火材料(图中部分产物没有列出)。
(1)固体甲与液体M反应的方程式为______。A溶液与固体H反应的离子方程式为______。
(2)固体乙的化学式为_______。液体M的电子式为_______。
(3)反应①~⑦中属于氧化还原反应的为_______(填写反应序号)。
(4)若I与C的稀溶液不反应,只能与G的浓溶液在加热条件下反应,则反应⑦的化学方程式为_______。
(5)若由黄铁矿(FeS2)与气体B反应来生产气体E,且每生成1 mol E放出426.5 kJ的热量,该反应的热化学方程式为_______ 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
(12分)已知金属单质A是生产生活中用量最大的金属。 D是难溶于水的白色固体。 F为红褐色固体。无色气体甲遇气体丙立即生成红棕色的气体乙。(图中部分产物和反应的条件略)。
请根据以上信息回答下列问题:
(1)写出下列物质的化学式C__________G__________。
写出反应①的化学方程式________________________________ 。
反应②的离子方程式_____________________________。
(3)反应④整个过程观察到的现象为_____________________________。
(4)反应⑤中,若将充满气体乙的试管倒扣在水槽中,充分反应后,试管内液体占试管总体积_______________。
(5)某种贫血症患者应补充C物质的阳离子。含该离子的药片外表包有一层特殊的糖衣,这层糖衣的作用就是保护该离子不被空气中的氧气氧化。为检验长期放置的药片已经失效,将药片去除糖衣后研碎,取少量研碎的药片放入烧杯中,加适量的蒸馏水,然后滴加数滴__________溶液,溶液显__________色,表明该药片已失效。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是无机物A~M在一定条件下的转化关系(部分产物及反应条件未列出)。其中,I是由第三周期元素组成的单质中熔点最高的金属,K是一种红棕色气体。
提示:4FeS2+11O2高温,2Fe2O3+8SO2
请填写下列空白:
(1)在周期表中,组成单质G的元素位于第________周期________族。
(2)在反应⑦中氧化剂与还原剂的物质的量之比为________。
(3)在②、③、⑥、⑨中既属于化合反应又属于非氧化还原反应的是________(填序号)。
(4)反应④的离子方程式是_____________________________________。
(5)将化合物D与KNO3、KOH共熔,可制得一种“绿色”环保高效净水剂K2FeO4(高铁酸钾),同时还生成KNO2和H2O。该反应的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
元素及其化合物在生产、生活中具有广泛的用途。
Ⅰ.铬化学丰富多彩.
(1)在常温下,铬能缓慢与稀硫酸反应,生成蓝色溶液。 与铜相比,其金属活泼性 (填“强”或“弱”);
⑵Cr( OH)3和Al( OH)3类似,也是两性氢氧化物,在水中存在酸式和碱式电离平衡,其酸式电离方程式是 ;
⑶工业上净化处理铬污染方法之一是:将含K2Cr2O7酸性废水放人电解槽内,加入适量的NaCl,以Fe和石墨为电极进行电解。经过一段时间后,生成Cr(OH)3和Fe(OH)3沉淀除去(已知KsP[ Fe(OH)3]=4.0×10-38,KsP[Cr(OH)3]=6.0×l0-31)。已知电解后的溶液中c( Fe3+)为2.0×10-13mol/L,则溶液中c(Cr3+)为 mol/L。
Ⅱ.物质A~H有如图所示转化关系(部分生成物未列出)。A、E、F、G均为气体,D为金属单质。
请回答下列问题:
(1)A的电子式为 D的化学式 ,C溶液的名称是 。
(2)反应①的化学方程式为 ;
反应③的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A~G各物质间的关系如下图,其中B、D为气态单质。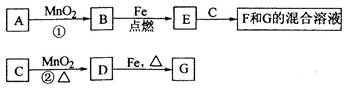
请回答下列问题:(①中MnO2作催化剂,②中MnO2作氧化剂)
(1)物质C和E的名称分别为________________、__________________;
(2)可选用不同的A进行反应①,若能在常温下进行,其化学方程式为_____________;若只能在加热情况下进行,则反应物A应为_____________;
(3)反应②的化学方程式:_______________________________________;
(4)新配制的F溶液应加入_____________以防止其转化为G。检验G溶液中阳离子的常用试剂是_____________,实验现象为____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com