
【题目】常温下,下列微粒能在相应溶液中大量共存的是( )
A.稀硫酸中:K+、MnO4﹣、CH3CH2OH
B.pH=11的溶液中:Na+、CO32﹣、NH3H2O
C.中性溶液中:Na+、NO3﹣、AlO2﹣
D.FeCl3溶液中:H2O2、Mg2+、SO42﹣
科目:高中化学 来源: 题型:
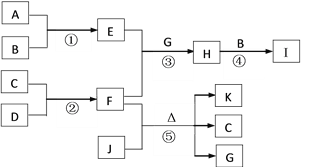
【题目】有关物质的转化关系如下图所示(反应条件未全部列出)。A、B、C、D、K为常见的单质,其中A为淡黄色固体,K为紫红色金属,B、C、D在常温常压下是气体,C在空气中含量最多。G为最常见的无色液体,反应③中F过量,I是常用化肥。请回答下列问题:
(1)G的电子式为______________。
(2)I的化学式为_______________。
(3)写出反应③的离子方程式:_________________。
(4)写出反应⑤的化学方程式:_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质空间构型和中心原子杂化类型都正确的是
A. CCl4 平面四边形 SP3 B. H2O V型 SP2
C. BCl3 平面三角形 SP2 D . NH4+ 正四面体 SP
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种工业废水中含有一定量的Cr2O72-和CrO42-,它们易被人体吸收积累而导致肝癌。污水处理厂常用还原沉淀法处理含铬废水,其流程如下:

(1)已知第①步存在平衡:2CrO42-(黄色)+2H+![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
① Cr2O72-中Cr的化合价是_______________。
② 常温下,若平衡体系的pH=10,则溶液显_________________色。
(2)第②步发生反应的离子方程式为__________,还原1 mol Cr2O72-离子,需要__________mol的FeSO4·7H2O;
(3)常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L,溶液的pH应调至______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、社会密切相关.下列说法中不正确的是( )
A.蛋白质、棉花、PVC,淀粉都是混合物
B.废弃的玻璃、金属、纸制品是可回收利用的资源
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D.用CO2合成聚碳酸酯可降解塑料,实现“碳”的循环利用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.1000 mol·L-1 HCl溶液滴定20.00 mL 0.100 0 mol·L-1 NH3·H2O溶液,滴定曲线如下图。下列说法不正确的是

A. ①溶液:c(NH3·H2O)+ c(NH![]() )=2c(Cl-)
)=2c(Cl-)
B. ①溶液:c(NH![]() )+2c(H+)=2c(OH-)+c(NH3·H2O)
)+2c(H+)=2c(OH-)+c(NH3·H2O)
C. ②溶液:c(NH![]() )=c(Cl-)>c(OH-)=c(H+)
)=c(Cl-)>c(OH-)=c(H+)
D. ③溶液:c(NH![]() ) > c(Cl-) > c(H+) > c(OH-)
) > c(Cl-) > c(H+) > c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿佛加德罗常数的值,下列说法正确的是( )
A. 标准状况下,将6.72L的NO2通入足量的水中转移电子数为0.3NA
B. 常温常压下,22.4LCCl4含有NA个CCl4分子
C. 1 mol Na与足量O2反应,生成Na2O和Na2O2混合物,转移的电子数为NA
D. 18 g D2O所含的电子数为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应中,元素X的原子将电子转移给元素Y的原子,则下列说法正确的是
①元素X被氧化 ②元素Y被氧化 ③元素X发生还原反应 ④元素Y发生还原反应
A. ①④ B. ③④ C. ②③ D. ①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列四组实验中现象或结论不正确的是

序号 | 实验现象 | 结 论 |
A | 热水中平衡球颜色比冷水中深 | 升温,化学平衡向吸热反应方向移动 |
B | 起始时产生气泡速率HCl > CH3COOH | 醋酸是弱电解质 |
C | 溶液颜色由黄变橙,且30秒内不变色 | 已达滴定终点 |
D | 划口处有蓝色沉淀 | 铁发生了析氢腐蚀 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com