


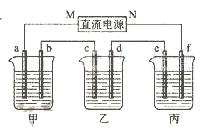
 (1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。
(1)接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加。 ①电源的N端为 极;
①电源的N端为 极; ②电极b上发生的电极反应为 ;
②电极b上发生的电极反应为 ; ③电极b上生成的气体在标准状况下的体积:
③电极b上生成的气体在标准状况下的体积:
 ④电极c的质量变化是 g;
④电极c的质量变化是 g; (2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?
(2)如果电解过程中铜全部析出,此时电解能否继续进行,为什么?  。
。 ⑤电解前后各溶液的pH如何变化。(填增大,减小或不变)
⑤电解前后各溶液的pH如何变化。(填增大,减小或不变) 甲溶液 ;
甲溶液 ; 乙溶液_______;
乙溶液_______; 丙溶液_______;
丙溶液_______;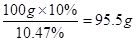 ,因此被电解的水是100g-95.5g=4.5g,物质的量是0.25mol,转移电子是0.25mol×2=0.5mol。所以生成氧气是0.125mol,标准状况下的体积是0.125mol×22.4L=2.8L。根据电子得失守恒可知,c电极析出铜是0.25mol,质量是0.25mol×64g/mol=16g。
,因此被电解的水是100g-95.5g=4.5g,物质的量是0.25mol,转移电子是0.25mol×2=0.5mol。所以生成氧气是0.125mol,标准状况下的体积是0.125mol×22.4L=2.8L。根据电子得失守恒可知,c电极析出铜是0.25mol,质量是0.25mol×64g/mol=16g。

科目:高中化学 来源:不详 题型:填空题
 __________________________________
__________________________________查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
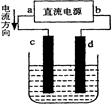
| A.a为正极、b为负极 |
| B.c为阳极、d为阴极 |
| C.电解过程中,溶液的碱性逐渐增强 |
| D.电解过程中,将湿润淀粉—KI试纸靠近d电极,看到试纸变蓝 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4(Cu(OH)2) | B.NaOH(NaOH) | C.NaCl(H2O) | D.CuCl2(CuCl2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.阳极上有红色固体析出 |
| B.总反应为;CuCl2+2H2O==Cu(OH)2+ H2↑+Cl2↑ |
| C.阴极反应为:2H++2e= H2↑ |
| D.阳极反应为:2Cl--2e= Cl2↑ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.精铜板作阴极,粗铜作阳极,CuSO4溶液作电解液 |
| B.电解时,阴极发生氧化反应,则阴极发生的反应为:Cu2+ +2e— ==Cu |
| C.粗铜中所含Ni.Fe.Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 |
| D.两电极质量变化值相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
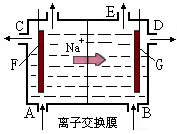
| A.从E口逸出的气体是H2 |
| B.从B口加入含少量NaOH的水溶液以增强导电性 |
| C.标准状况下每生成22.4 LCl2,便产生2 mol NaOH |
| D.F电极材料为金属铁 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com