
【题目】海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
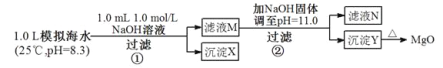
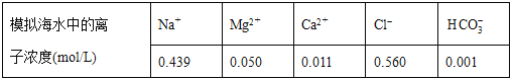
注:溶液中某种离子的浓度小于1.0×10-5mol/L,可认为该离子不存在;实验过程中,假设溶液体积不变。
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12。下列说法正确的是( )
A. 沉淀物X为CaCO3
B. 滤液M中存在Mg2+,不存在Ca2+
C. 滤液N中存在Mg2+,Ca2+
D. 步骤②中若改为加入4.2 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物
【答案】A
【解析】
步骤①发生Ca2++OH―+HCO3-![]() CaCO3↓+H2O;步骤②:Ksp[Mg(OH)2]=c(Mg2+)×(10-3)2=5.6×10-12,c(Mg2+)=5.6×10-6。Q[Ca(OH)2]=c(Ca2+)×(10-3)2=10-8<Ksp,无Ca(OH)2析出。A、生成0001 mol CaCO3,选项A正确;B 、剩余c(Ca2+)=0.001 mol/L,选项B错误;C、c(Mg2+)=5.6×10-6<10-5,无剩余,选项C错误;D、生成0.05 mol Mg(OH)2,余0.005 mol OH―,Q[Ca(OH)2]=0.01×0.0052=2.5×10-7<Ksp,无Ca(OH)2析出,选项D错误。答案选A。
CaCO3↓+H2O;步骤②:Ksp[Mg(OH)2]=c(Mg2+)×(10-3)2=5.6×10-12,c(Mg2+)=5.6×10-6。Q[Ca(OH)2]=c(Ca2+)×(10-3)2=10-8<Ksp,无Ca(OH)2析出。A、生成0001 mol CaCO3,选项A正确;B 、剩余c(Ca2+)=0.001 mol/L,选项B错误;C、c(Mg2+)=5.6×10-6<10-5,无剩余,选项C错误;D、生成0.05 mol Mg(OH)2,余0.005 mol OH―,Q[Ca(OH)2]=0.01×0.0052=2.5×10-7<Ksp,无Ca(OH)2析出,选项D错误。答案选A。


科目:高中化学 来源: 题型:
【题目】已知反应A+B=C+D的能量变化如图所示(E1、E2均为正值),下列说法正确的是
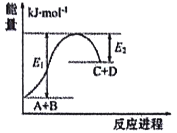
A. 破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
B. 该反应只有在加热条件下才能进行
C. A和B的总能量一定高于C和D的总能量
D. 该反应吸收的能量为(E1-E2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是( )
① 金属先熔化 ② 在空气中燃烧,产生苍白色火焰 ③ 燃烧后得白色固体
④ 燃烧时火焰为黄色 ⑤ 燃烧后生成浅黄色固体物质
A. ② ⑤ B. ①②③ C. ①④⑤ D. ④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将下图所示实验装置的 K 闭合,下列判断正确的是
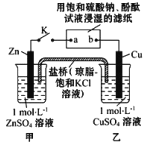
A.片刻后甲池中 c(SO42-)增大 B.电子沿 Zn→a→b→Cu 路径流动
C.Cu 电极上发生还原反应 D.片刻后可观察到滤纸 b 点变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】咖啡酸具有止血功效,存在于多种中药中,其结构简式如图,下列有关说法正确的是

A. 该物质中苯环上一氯代物有2种
B. 1 mol该物质可以与1.5 mol碳酸钠溶液反应生成1.5 mol CO2
C. 1 mol该物质可以和4 mol浓溴水发生反应
D. 所有碳原子不可能都在同一个平面上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型熔融盐燃料电池具有高发电效率.现用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通入CO气体,另一极通入O2和CO2混合气体,其总反应为:2CO+O2===2CO2 . 则下列说法中正确的是
A. 通CO的一极是电池的正极
B. 负极发生的电极反应是:O2+2CO2+4e-===2CO![]()
C. 负极发生的电极反应是:CO+CO![]() -2e-===2CO2
-2e-===2CO2
D. 通O2的一极做阴极,发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的数目是
①12.0g熔融的NaHSO4中含有的阳离子数为0.2NA
②1mol Na2O 和Na2O2混合物中含有的阴、阴离子总数是3NA
③常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
④7.8g![]() 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA
⑤用1L1.0 mol/LFeCl3溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为NA
⑥1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2NA个电子
⑦在反应KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2转移的电子数为5NA
⑧常温常压下,17 g甲基(-14CH3)中所含的中子数为9NA
A. 3 B. 4 C. 5 D. 6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示(电极材料为石墨)。

(1)图中a极要连接电源的_____(填“正”或“负”)极,SO![]() 放电的电极反应_____________。
放电的电极反应_____________。
Ⅱ.在如图所示的装置中,若通入直流电5 min时,铜电极质量增加2.16 g,试回答:
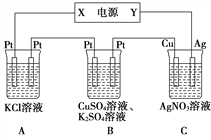
(2)溶液pH变化: B________,C________(填“增大”“减小”或“不变”)。
(3)通电5 min时,B中共收集224 mL气体(标准状况),溶液体积为200 mL。则通电前CuSO4溶液的物质的量浓度为________(设电解前后溶液体积无变化)。
(4)若A中足量的KCl溶液的体积也是200 mL,电解后,溶液的pH为_____(设电解前后溶液体积无变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质混合后,不能生成NaOH的是
A.Na和H2OB.Ca(OH)2溶液和NaCl溶液
C.Na2O2和H2OD.Ca(OH)2溶液和Na2CO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com