
【题目】A、B、C、D、E是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下:
元素 | 相关信息 |
A | 基态原子的价电子排布式为nSnnPn |
B | 元素原子的核外p电子数比s电子数少1个 |
C | 最外层电子数是电子层数的3倍 |
D | 简单离子是第三周期元素中离子半径最小的 |
E | 价电子层中的未成对电子数为4 |
请回答下列问题:
(1)写出下列元素的名称:A______, B_______, C________,D__________
(2)写出C元素在周期表的位置_________,E2+价电子的轨道表示式________________,B元素能量最高的电子为_____轨道上的电子,其轨道呈_______形.
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物中σ键有______个,π键有______个。
(4)B、C、D的简单离子的半径由大到小的顺序为_____________(用离子符号表示)。
(5)写出C的核外有18个电子的氢化物的电子式_____________。
【答案】 碳 氮 氧 铝 第2周期第VIA族 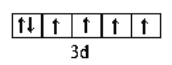 2p 纺锤形(或哑铃形) 2
2p 纺锤形(或哑铃形) 2 ![]() 2
2![]() N3->O2->Al3+
N3->O2->Al3+ ![]()
【解析】A元素基态原子的价电子排布式为nsnnpn,则n=2,所以A是碳元素;D元素简单离子是第三周期元素中离子半径最小的,则D是Al元素;C元素最外层电子数是电子层数的3倍,原子序数小于Al,则C是氧元素;元素B原子的核外p电子数比s电子数少1个,比铝的原子序数小,因此B是N;E元素价电子层中的未成对电子数为4,则E的价层电子排布是3d64s2,即为铁元素;
(1)根据以上分析可知,各元素的名称分别为:A为碳;B为氮,C为氧,D为铝;正确答案:碳;氮 ; 氧; 铝。
(2)C元素为氧,核电荷数为8,位于周期表第2周期第VIA族;E为铁,核电荷数为26,Fe2+价电子的轨道表示式 ;B为氮,核外电子排布为1s2 2s2 2p3,因此能量最高的电子为2p轨道上的电子,其轨道呈纺锤形(或哑铃形)形。正确答案:第2周期第VIA族;
;B为氮,核外电子排布为1s2 2s2 2p3,因此能量最高的电子为2p轨道上的电子,其轨道呈纺锤形(或哑铃形)形。正确答案:第2周期第VIA族;  ;2p; 纺锤形(或哑铃形)。
;2p; 纺锤形(或哑铃形)。
(3)按原子轨道的重叠方式,1molA与C形成的最高价化合物为二氧化碳,为共价化合物,碳氧之间为双键,因此1mol二氧化碳分子中含有σ键有2 ![]() 个;π键有2
个;π键有2![]() 个;正确答案:2
个;正确答案:2 ![]() ; 2
; 2![]() 。
。
(4)B、C、D的简单离子分别为N3-、O2-、Al3+,核外电子排布相同的离子,核电荷数越大,离子半径越小,因此离子半径由大到小的顺序为N3->O2->Al3+;正确答案:N3->O2->Al3+。
(5)氧元素的核外有18个电子的氢化物是双氧水,属于共价化合物,电子式为![]() ;正确答案:
;正确答案:![]() 。
。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.可用酸性KMnO4溶液区鉴别甲烷和乙烯
B.乙烯使酸性KMnO4溶液和溴水褪色的原理相同
C.X气体通入溴水中,溴水褪色,则X气体一定为乙烯
D.甲烷易发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用KMnO4和浓盐酸反应制取氯气:KMnO4+HCl(浓)=KCl+MnCl2+Cl2↑+H2O(未配平)。
(1)配平化学方程式,并用单线桥标出电子转移的方向和数目____________。
(2)将上述配平的化学方程式改写为离子方程式________________________。
(3)浓盐酸在反应中显示出来的性质是____________。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(4)若产生0.5 mol Cl2,则被氧化的HCl_______mol,转移的电子的数目约为____。
(5)一定条件下,KMnO4还可以氧化其他还原性物质。__MnO4-+ C2O42-+ = Mn2++ CO2↑+ ,完成上述离子方程式,此反应中,发生氧化反应的物质是______;若转移1 mol电子,生成标准状况下CO2_____L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
①1L0.1mol/LNH4NO3溶液中氮原子数小于0.2NA
②用标准盐酸滴定NaOH 溶液测其浓度时,酸式滴定管用蒸馏水洗涤后,没用标准盐酸润洗,直接装标准盐酸滴定,所测的碱液浓度偏低
③PH相等的四种溶液: a.CH3COONa b.C6H5ONa c.NaHCO3 d.NaOH。(已知酸性:C6H5OH2CO3),其溶液物质的量浓度由小到大顺序为:d、b、c、a
④钢铁腐蚀时可能发生的正极反应: 2H2O+O2+4e-=4OH-
⑤电解饱和MgCl2溶液时,电解反应式为:2H2O+2Cl-![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
⑥在海轮外壳连接锌块保护外壳不受腐蚀是采用牺牲阳极的阴极保护法
⑦长期使用硫酸铵,土壤酸性增强:草木灰与铵态氮肥不能混合施用
A. ①②⑤⑥ B. ①③⑤⑦ C. ②③④⑤ D. ③④⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50g溶质质量分数为w1,物质的量浓度为c1 的较浓氨水沿玻璃棒加人到u mL水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀氨水。若c1 =2c2,则:
A. w1>2w2,u>50 B. w1<2w2,u<50 C. w1=2w2,u<50 D. w1<2w2,u>50
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是一门以实验为基础的学科,下列操作或发生事故时的处理方法正确的是
A. 可用燃着的酒精灯引燃另一只酒精灯。
B. 给试管里的液体加热时,试管应与桌面垂直。
C. 配置一定浓度的NaCl溶液时,定容振荡摇匀后,发现液面低于刻度线,再加水到刻度线。
D. 浓硫酸不慎沾在皮肤上,应立即用大量水冲洗,最后涂上3%-5%的小苏打溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:
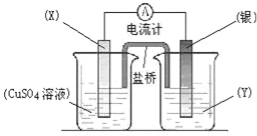
(1)电极X的材料是 (化学式);电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com