
【题目】某无色溶液能与铝作用生成氢气,则溶液中可能大量共存的离子组是( )
A. H+、Ba2+、MnO4-、Cl- B. Cl-、CO32-、Cu2+、Mg2+
C. NO3-、SO42-、K+、H+ D. NO3-、OH-、Ba2+、Cl-
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g)![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g)![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2L的密闭容器中充入8mol N2O5 (g),加热到t℃,达到平衡状态后,O2为9mol, N2O3 为3.4mol,则t‘C时反应①的平衡常数为( )
A.10.7 B.8.5 C.9.6 D.10.2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“化学与生活”的说法不正确的是( )
A.硫酸钡可用作钡餐透视
B.盐卤可用于制豆腐
C.明矾可用于水的消毒,杀菌
D.醋可用于除去暖水瓶中的水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中物质的分类组合完全正确的是
A | B | C | D | |
酸 | H3PO4 | CH3COOH | NaHSO4 | HNO3 |
碱 | Mg(OH)Cl | NaOH | Fe(OH)3 | KOH |
盐 | CuSO45H2O | BaSO4 | NaH2PO4 | Na2S |
氧化物 | H2O | KClO3 | CuO | H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是

A. 原子半径:X<Y<Z
B. 气态氢化物的稳定性:X>Z
C. 最高价氧化物对应水化物的酸性:Y>W
D. Z、W均可与Mg形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:

(1)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化的曲线是 填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为 m2。 则 m1 m2 ( 选填“<”、“=”、“>”)。[来
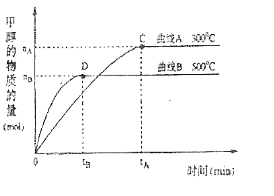
(2)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g) ![]() CH3OH(g)。升高温度,K值 (填“增大”、“减小”或“不变”)。在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。
CH3OH(g)。升高温度,K值 (填“增大”、“减小”或“不变”)。在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。
(3)某温度下Ksp[ Mg(OH)2] = 2×10 -11,若该温度下某MgSO4溶液里c(Mg 2+) =0.002 mol·L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于 ;该温度下,在0.20L的0.002mol/LMgSO4溶液中加入等体积的0.10mol/L的氨水溶液,该温度下电离常数Kb(NH3·H2O)=2×10-5,试计算 (填“有”或“无”) Mg(OH)2沉淀生成?
(4)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人们对原子结构的认识有一个不断深入的过程,下列先后顺序中符合化学史实的是( )
①道尔顿提出的原子论 ②卢瑟福的原子结构行星模型 ③波尔提出的原子力学模型 ④汤姆生提出的葡萄干面包原子模型 ⑤现代量子力学模型
A. ①②④⑤③ B. ①④②③⑤ C. ②①④⑤③ D. ①③⑤②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com