
【题目】【化学——选修化学与技术】
(1)纯碱是一种重要的化工原料。目前制碱工业主要有“氨碱法”和“联合制碱法”两种工艺。
①“氨碱法”产生大量CaCl2废弃物,写出该工艺中产生CaCl2的化学方程式:_________________;
②写出“联合制碱法”有关反应的化学方程式:_____________________;
③CO2是制碱工业的重要原料,“联合制碱法”与“氨碱法”中CO2的来源有何不同?_________________;
(2)钢铁工业对促进经济和社会发展起了重要作用。
① 炼钢时,加入硅、锰和铝的目的是_______________________________。
② 不锈钢含有的Cr元素是在炼钢过程的氧吹____________(填“前”或“后”)加入。
③ 炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作__________________。
【答案】(1)①2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O (2分)
2NH3↑+CaCl2+2H2O (2分)
② NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl(2分)
2NaHCO3![]() Na2CO3+CO2↑+H2O (2分)(或写总反应方程式:2NaCl+2NH3+CO2+H2O=Na2CO3+2NH4Cl)
Na2CO3+CO2↑+H2O (2分)(或写总反应方程式:2NaCl+2NH3+CO2+H2O=Na2CO3+2NH4Cl)
③“氨碱法”CO2来源于石灰石煅烧,“联合制碱法”CO2来源于合成氨工业的废气;(2分)
(2)① 脱氧和调整钢的成分 (2分)② 后 (1分)③ CO (2分) 燃料(或还原剂) (2分)
【解析】
试题分析:(1)①氨碱法工艺中产生大量CaCl2是由氯化铵和消石灰在加热条件下反应后生成氨气和氯化钙的反应,反应的化学方程式为2NH4Cl+Ca(OH)2![]() 2NH3↑+CaCl2+2H2O;
2NH3↑+CaCl2+2H2O;
②联合制碱法是在氨的饱和NaCl溶液中二氧化碳气体,反应生成碳酸氢钠,解热碳酸氢钠即可制备碳酸钠,反应的有关方程式为,NH3+CO2+H2O+NaCl(饱和)=NaHCO3↓+NH4Cl、2NaHCO3![]() Na2CO3+CO2↑+H2O,总反应方程式:2NaCl+2NH3+CO2+H2O=Na2CO3+2NH4Cl;
Na2CO3+CO2↑+H2O,总反应方程式:2NaCl+2NH3+CO2+H2O=Na2CO3+2NH4Cl;
③CO2是制碱工业的重要原料,联合制碱法中CO2来源于石灰石煅烧,氨碱法中CO2的来源于合成氨工业的废气;
(2)①炼钢时,加入硅、锰和铝,可与氧气反应,且能改变合金的性质,起到脱氧和调整钢的成分的作用;②因为Cr易被氧化,为Cr被氧化,不锈钢含有的Cr元素是在炼钢过程的氧吹后,若氧吹前加入Cr会形成炉渣被除去;
③炼铁和炼钢生产中,CO是主要的还原剂,故尾气均含有的主要污染物是CO,一氧化碳会引起中毒,故需对其进行尾气处理.一氧化碳是一种很好的还原剂同时还是一种燃料。


 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:
【题目】化学与生活、生产、可持续发展密切相关,下列说法正确的是
A. 14C可用于文物年代的鉴定,14C和12C互为同素异形体
B. 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因
C. 现代工业生产中芳香烃主要来源于石油化工的催化重整和煤的干馏
D. 高纯度的SiO2可以制成光电池将光能直接转换为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
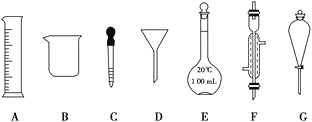
(1)写出仪器名称:D________,F________。
(2)下列实验操作中用到仪器G的是________(填下列选项的编号字母)。]
a.分离水和CCl4的混合物 b.分离水和酒精的混合物 c.分离水和泥沙的混合物
(3)实验室需要配制450mL 0.4 mol/L的硫酸溶液。
①配制时,实验室提供了以下仪器:烧杯、100mL量筒、玻璃棒、托盘天平(带砝码)、胶头滴管,还缺少的玻璃仪器是 。上述实验中使用容量瓶前必须进行的操作是
②配制该溶液需用98﹪的浓硫酸(密度为1.8g/mL)___________mL。取用该体积浓硫酸时,需要用到上述仪器中的A和___________(填仪器的编号字母)。
③下列操作会使配制的溶液浓度偏高的是________(填下列选项的编号字母)。
A.转移过程中有少量溶液溅出 |
B.没有冷却,立即转移到容量瓶中定容 |
C.摇匀后,液面下降,补充水 |
D.定容时俯视刻度线 |
E.量筒量取浓硫酸是仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果。下列表达不正确的是
A.分散质粒子直径与分散系种类:![]()
B.NaOH溶液与CO2反应后溶液中的钠盐:
C.AlCl3溶液中滴加NaOH溶液后铝的存在形式:![]()
D.Na与O2反应的产物:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中:①CO2②Ar、③SiO2、④NaOH、⑤NaF、⑥KOH、⑦CaCl2、⑧Na2O2、⑨H2O、⑩N2 , 只含有共价键的物质是;只含有离子键的物质是;既含有离子键,又含有共价键的是;不存在化学键的是 . (填写序号)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修物质结构与性质】已知A、B、C、D、E五种元素的原子序数依次增大,其中A、E原子的最外层电子数均等于其周期序数,E原子的电子层数是A的3倍;B原子核外电子有6种不同的运动状态,S轨道电子数是P轨道电子数的两倍;D原子L层上有2对成对电子。请回答下列问题:
(1)E元素基态原子的电子排布式为___________________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为_____________(填元素符号)。
(3)D元素与氟元素相比,电负性:D_______________F(填“>”、“=”或“<”)。
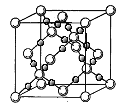
(4)BD2在高温高压下所形成的晶体其晶胞如图所示。该晶体的类型属于___________________(选填“分子”、“原子”、“离子”或“金属”)晶体,该晶体中B原子轨道的杂化类型为_____________。l mol B2A2分子中含![]() 键的数目是_________________。
键的数目是_________________。
(5)光谱证实单质E与强碱溶液反应有[E(OH)4]—生成,则[E(OH)4]—中存在____________。
a.共价键 b.配位键 c.σ键 d.π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Fe2+检验的方法正确的是
A. 滴加氢氧化钠溶液 B. 先滴加KSCN溶液,再滴加盐酸
C. 滴加KSCN溶液 D. 先滴加氯水,再滴加KSCN溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com