
A、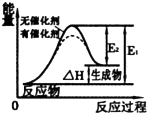 图表示催化剂能改变化学反应的焓变 |
B、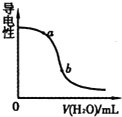 图表示向氨水中加水时溶液导电性的变化情况,且溶液c(OH-)大小:a<b |
C、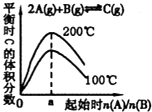 由图可知反应2A(g)+B(g)?C(g)的△H>O,且 a=2 |
D、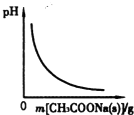 图表示向CH3COOH溶液中逐渐加入CH3COONa固体后,溶液pH的变化情况 |


 天天向上口算本系列答案
天天向上口算本系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp[CaSO4] |
| B、Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
| C、已知25℃时,Ksp[Fe(OH)3]=4.0×10-38,该温度下反应Fe(OH)3+3H+?Fe3++3H2O的平衡常数K=4.0×104 |
| D、已知25℃时,Ksp[Mg(OH)2]=1.8×10-11,在MgCl2溶液中加入氨水,测得混合液的pH=11,则溶液中的c(Mg2+)为1.8×10-3mol.L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 光 |
| Br2 |
| NaOH,醇 |
| △ |
| Br水 |
| NaOH,H2O |
| O2,催化剂 |
| △ |
| O2,催化剂 |
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 3-n |
| 2 |
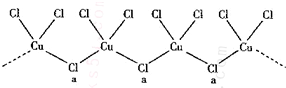
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol FeI2与足量氯气反应时转移的电子数为2NA |
| B、标准状况下,5.6L丙烷中含有共价键的数目为2NA |
| C、16g由氧气和臭氧组成的混合物中含有的分子总数为0.5 NA |
| D、0.1 mol乙烯和乙醇的混合物完全燃烧所消耗的氧原子数一定为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、整个反应过程中:c(H+)+c(Na+)+c(NH4+)=c(OH-)+2c(SO42-) |
| B、当滴入30mL NaOH溶液时(pH>7):c(NH4+)>c(NH3?H2O)>c(OH-)>c(H+) |
| C、当滴入20mL NaOH溶液时:2c(SO42-)=c(NH3?H2O)+c(NH4+) |
| D、当溶液呈中性时:c(NH4+)>c(SO42-)>c(Na+)>c(H+)=c(OH-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com