


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、①③④ | B、②③④ |
| C、①②③④ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
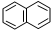 或
或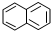 ,两者是等同的.苯并[α]芘是强致癌物,其分子由5个苯环拼和而成,可表示为如下(1)或(2),这两者也是等同的.现有(A)到(D)
,两者是等同的.苯并[α]芘是强致癌物,其分子由5个苯环拼和而成,可表示为如下(1)或(2),这两者也是等同的.现有(A)到(D)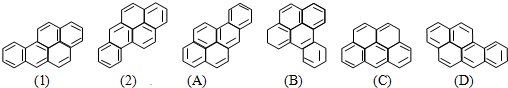
查看答案和解析>>
科目:高中化学 来源: 题型:
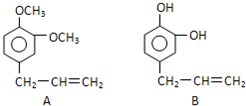 从某些植物树叶提取的挥发油中含有下列主要成分:
从某些植物树叶提取的挥发油中含有下列主要成分:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钛合金与人体具有很好的“相容性”,可以用来制造人造骨骼 |
| B、铁具有良好的导热性,可以用于制造炊具 |
| C、不锈钢抗腐蚀性好,常用于制造医疗器械 |
| D、铅锑合金的熔点较低、电阻率较大,常用于制成发热体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com