
【题目】已知热化学方程式:C(S,金刚石)+ O2(g)=CO2(g);ΔH=![]() 395.41KJ/mol
395.41KJ/mol
C(S,石墨)+ O2(g)=CO2(g);ΔH=![]() 393.51KJ/mol
393.51KJ/mol
则金刚石转化为石墨的热化学方程式为___________________,由热化学方程式看更稳定的碳的同素异形体是_________________________。
【答案】C(S,金刚石)=C(S,石墨);△H=-1.9KJ/mol石墨
【解析】
根据金刚石和石墨燃烧的热化学方程式,利用盖斯定律二式相减可得金刚石转化为石墨的热化学方程式,据此进行解答。
已知:①C(s,石墨)+O2(g)═CO2(g)△H=-393.51kJmol-1
②C(s,金刚石)+O2(g)═CO2(g)△H=-395.41kJmol-1
利用盖斯定律将②-①可得:C(s,金刚石)═C(s,石墨);△H=(-395.41kJmol-1)-(-393.51kJmol-1)=-1.9kJmol-1,故答案为:C(s,金刚石)═C(s,石墨)△H=-1.9kJmol-1;物质所含能量越低越稳定,由热化学方程式看更稳定的碳的同素异形体是石墨。


科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应2SO2+O2![]() 2SO3,反应达平衡的标志是
2SO3,反应达平衡的标志是
①单位时间内消耗2 mol SO2的同时生成2 mol SO3
②反应混合物中,SO2、O2与SO3的物质的量之比为2∶1∶2
③反应混合物中,SO3的质量分数不再改变
A. ①②B. ①③C. ①D. ③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组用右图装置进行实验,试回答:
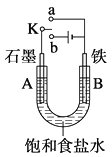
(1)若开始时开关K与a连接,则A电极反应式为________。
(2)若开始时开关K与b连接,这种方法经常用于金属的防护,这种防护措施叫做________,则A电极反应式为________;B电极反应式为________。
(3)开关K与b连接,将饱和食盐水换成CuSO4溶液,则A电极反应式为________,该反应的离子方程式为________ ,若将电解质溶液恢复至原状,应补充________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将氨水缓缓地滴入盐酸中至中性,下列有关的说法:①盐酸过量 ②氨水过量 ③恰好完全反应 ④c (NH4+) = c(Cl-) ⑤c (NH4+) < c(Cl-) 正确的是
A.②④B.③④C.②⑤D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①C(s)+O2(g)=CO2(g);ΔH=![]() 393.5kJ/mol
393.5kJ/mol
②2CO(g) +O2(g)=2CO2(g);ΔH=![]() 566kJ/mol
566kJ/mol
③CaCO3(s)=CaO(s)+CO2(g);ΔH=![]() 177.7kJ/mol
177.7kJ/mol
④0.5H2SO4(l) +NaOH(l)=0.5Na2SO4(l)+H2O(l);ΔH=![]() 57.3kJ/mol
57.3kJ/mol
⑤HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l);ΔH=![]() 57.3kJ/mol
57.3kJ/mol
(1)上述热化学方程式中,不正确的有___________________(填序号,以下同);
(2)上述反应中,表示燃烧热的热化学方程式是___________________________________;上述反应中,表示中和热的热化学方程式是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证木炭可被浓H2SO4氧化成CO2,选用下图所示仪器(内含物质)组装成实验装置:

(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
接 , 接 , 接 ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?
乙中 ____ ,丙中 ______ ;
(3)丁中酸性KMnO4溶液的作用是 ;
(4)写出甲中反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过,下列有关叙述正确的是

A. 铜电极上发生氧化反应
B. 电池工作一段时间后,甲池的c(SO42-)减小
C. 电池工作一段时间后,乙池溶液的总质量增加
D. 阴阳离子离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种短周期元素,其原子序数依次增大,其中:C元素的原子最外层电子数是次外层电子数的三倍;A与D、C与F同主族;D是所在周期原子半径最大的主族元素,又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)元素D在周期表中的位置________________。
(2)写出B单质的电子式________________。
(3)C、D、F三种元素形成的简单离子的半径由大到小的顺序是________(用离子符号表示)。
(4)由A、B、C三种元素以原子个数比4∶2∶3形成化合物X,X中所含化学键类型有_________________________。
(5)若E是金属元素,其单质与氧化铁反应常用于焊接钢轨,请写出反应的化学方程式:________________________________________________;若E是非金属元素,其单质在电子工业中有重要应用,请写出其氧化物溶于强碱溶液的离子方程式:______________________________________________。
(6)FC2气体有毒,排放到大气中易形成酸雨,写出FC2与氧气和水蒸气反应的化学方程式_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图示与对应的叙述符合的是
A. 如图可知实线、虚线分别表示某可逆反应未使用催化剂和使用催化剂的正、逆反应速率随时间的变化

B. 如图可知,反应C(金刚石,s) ══ C(石墨,s)的焓变ΔH ══ ΔH1-ΔH2

C. 如图可知表示除去氧化膜的镁条放入盐酸中生成氢气速率随时间的变化,起初反应速率加快的原因可能是该反应为放热反应

D. 如图可知表示25℃时用0.1000 mol·L-1醋酸滴定40.00 mL 0.1000 mol·L-1NaOH溶液得到的滴定曲线

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com