
| A���٢� | B���٢� | C���ڢ� | D���ڢ� |
 ������������ϵ�д�
������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
| ʵ�� ��� | �¶�/K | ����Ũ�� /mol��L-1 | ����Ũ��/mol��L-1 | ʵ��Ŀ�� |
| �� | 298 | 0.20 | | a.ʵ��ٺ͢ڣ�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죻 b.ʵ��ٺۣ͢�̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻 c.ʵ��ܢݣ�̽���¶ȶ�þ�����ᷴӦ��þ����ᷴӦ���ʵ�Ӱ�죬�ĸ�����һЩ�� |
| �� | 308 | 0.20 | | |
| �� | 298 | 0.40 | | |
| �� | | 0.20 | 0.20 | |
| �� | | | |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 4Y(g)��Z(g)����H<0����ij�¶�ʱ
4Y(g)��Z(g)����H<0����ij�¶�ʱ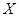 ��Ũ����ʱ��仯�����ߣ�
��Ũ����ʱ��仯�����ߣ�
A����6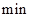 ��Ӧ����ֹ�� ��Ӧ����ֹ�� |
| B��X�ڵ�һ���Ӻ͵ڶ������ڵ� ƽ����Ӧ����֮����3:2 |
| C���÷�Ӧ�Ĺ������ؼ�С�Ĺ��� |
| D���������¶ȣ�v������v������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����죬5%H2O2��Һ�ֽ� | B�����죬MnO2��5%H2O2��Һ��� |
| C�����죬5%H2O2��Һ�ֽ� | D�����죬MnO2��5%H2O2��Һ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 ���ڿ�ʼʱ��Ӧ�ٶ�
���ڿ�ʼʱ��Ӧ�ٶ�
 ����������Ӧ��ƽ���ٶ�
����������Ӧ��ƽ���ٶ�
| A���ۢܢݢ� | B���٢ۢޢ� | C���٢ڢۢ� | D���ڢۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

| A�������¶� | B��ͨ�˺���ʹ��ѹǿ���� | C�����������г���N2O4 | D��ʹ�ô��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)+H2O(g);�SH<0��Ϊ��̽���䷴Ӧԭ����������ʵ�飬��2L�ܱ�������250�������£����n(CO2)��ʱ��ı仯������±���
CH3OH(g)+H2O(g);�SH<0��Ϊ��̽���䷴Ӧԭ����������ʵ�飬��2L�ܱ�������250�������£����n(CO2)��ʱ��ı仯������±���| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO2)(mol) | 0.40 | 0.35 | 0.31 | 0.3 | 0.3 | 0.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g)�����2min��N2��Ũ����6mol/L��С��2mol/L����ô��N2Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����2min�ڵķ�Ӧ����Ϊ
2NH3(g)�����2min��N2��Ũ����6mol/L��С��2mol/L����ô��N2Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����2min�ڵķ�Ӧ����Ϊ| A��4 mol/L | B��2mol/(L��min) | C��6 mol/(L��min) | D��3mol/(L��min) |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com