
在2L密闭容器中进行的反应2SO2(g)+O2(g) 2SO3(g),在10秒内反应物SO2的物质的量由1mol降到0.6mol,则反应速率ν(O2)为( )
2SO3(g),在10秒内反应物SO2的物质的量由1mol降到0.6mol,则反应速率ν(O2)为( )
A.0.02mol/(L·s) B.0.04mol/((L·s) C.0.01mol/((L·s) D.0.2mol/((L·s)
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:填空题
(8分)(1)苯氯乙酮是一具有荷花香味且有强催泪作用的化学试剂,它的结构简式如图所示,则苯氯乙酮不可能具有的化学性质是 (填字母序号)。
a.加成反应 b.取代反应 C.消去反应d.水解反应 e.银镜反应 f.还原反应
(2)由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。

①聚合物F的结构简式: 。
②c与新制的Cu(OH) 碱性悬浊液共热转化为D的化学方程式是: 。
碱性悬浊液共热转化为D的化学方程式是: 。
③在一定条件下,两分子E能脱去两分子水形成一种六元环状化合物,该化合物的结构简式是: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是( )
A.向银氨溶液中加入盐酸:[Ag(NH3)2]++OH—+3H+=Ag++2NH4++H2O
B.NaHCO3溶液和少量Ba(OH)2溶液混合:HCO3— +OH—+Ba2+=H2O+BaCO3↓
C.硫酸铝溶液显酸性:Al3++3H2O Al(OH) 3↓+3H+
Al(OH) 3↓+3H+
D.在少量Mg(OH)2悬浊液中滴加氯化铵浓溶液:Mg(OH)2+2NH4+=2NH3·H2O+Mg2+
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
某元素只存在两种天然同位素,且在自然界它们的含量相近,其相对原子质量为152.0,原子核外的电子数为63。下列叙述中错误的是( )
A.它是副族元素 B.它是第六周期元素
C.它的原子核内有63个质子 D.它的一种同位素的核内有89个中子
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列变化过程中,只破坏共价键的是( )
A.I2升华 B.NaCl颗粒被粉碎
C.HCl溶于水得盐酸 D.从NH4HCO3中闻到了刺激性气味
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市高三六校第二次联考理综化学试卷(解析版) 题型:填空题
【化学——选修2化学与技术】
生产自来水的流程图所示。

(1) FeSO4·7H2O是常用的混凝剂,它在水中最终生成 沉淀。
(2)实验室过滤操作所用到的玻璃仪器是 。
(3)我们有时感觉自来水“有漂白粉的气味”,是因为使用了氯气消毒,请写出有关化学方程下列物质中, (填写序号)可以作为氯气的代用品。
①臭氧 ②NH3(溶液) ③K2FeO4 ④SO2
(4)有些地区的天然水中含有较多的钙、镁离子。用离子交换树脂软化硬水时,先后把水通过分别装有 离子交换树脂和 离子交换树脂的离子交换柱(填“阴”或 “阳”)。
(5)测定水中的溶解氧:量取20mL水样,迅速加入MnSO4和KOH的混合溶液,再加入KI溶液,立即塞好塞子,振荡使其完全反应。打开塞子,迅速加入适量硫酸溶液,此时有碘单质生成。用0.010mol/L Na2S2O3溶液滴定生成的碘,消耗了6.00mL Na2S2O3溶液。已知在碱性溶液中,氧气能迅速氧化Mn2+,生成物在酸性条件下可以将碘离子氧化为碘单质,本身重新还原为Mn2+。
上述过程发生的反应可表示为:
2Mn2++4OH-+O2=2MnO(OH)2
MnO(OH)2+2I-+4H+=I2+Mn2++3H2O
I2+2S2O32-=2I-+S4O62-
水中的溶解氧量为 (以mg·L-l为单位)。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市第二学期期末教学质量测试高二化学试卷(解析版) 题型:简答题
由短周期元素组成的甲?乙和丙均为中学常见物质,一定条件下,存在转化关系:
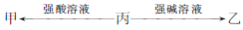
(1)若甲?乙?丙都是单质,甲?乙是同种气体,丙元素的原子结构示意图为 ;丙单质性质活泼,但由其制成的容器可用于储运浓硫酸,原因是 ?工业中制取丙的化学方程式:
(2)若甲?乙是同种有机物,体积分数为75%该有机物的水溶液常用于医疗消毒?写出分子中含有4个碳原子的丙转化为甲的化学方程式:
(3)若甲?乙是不同种气体,乙能使湿润的红色石蕊试纸变蓝?
①写出丙→甲反应的离子方程式: (任写一个)
②0.1mol乙与CuO(s)完全反应,得到一种气态单质?一种固态单质和一种液态化合物,放出14.7kJ的热量?该反应的热化学方程式为 ?
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:实验题
(12分)某学生用0.1000mol·L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为以下几步:
A移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B用标准NaOH溶液润洗滴定管2~3次
C把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面至“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)下图中属于碱式滴定管的 (选填:“甲”、“乙”)。

(2)正确的操作顺序是 (填字母序号)。
(3)上述B步操作的目的是 。
(4)判断到达滴定终点的实验现象是 。
(5)上述A步操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是 (填“偏大”或“偏小”或“无影响”)。
(6)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
试计算待测盐酸的物质的量浓度(列出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com