
(12分)某学生用0.1000mol·L-1标准NaOH溶液滴定未知浓度的盐酸,其操作可分解为以下几步:
A移取25.00mL待测盐酸溶液注入洁净的锥形瓶中,并加入2~3滴酚酞溶液
B用标准NaOH溶液润洗滴定管2~3次
C把盛有标准NaOH溶液的碱式滴定管固定好,挤压玻璃珠,使滴定管尖嘴充满溶液
D取标准NaOH溶液注入碱式滴定管到“0”刻度以上2~3cm
E.调节液面至“0”或“0”刻度以下,记下读数
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定到终点,并记下滴定管液面的读数
(1)下图中属于碱式滴定管的 (选填:“甲”、“乙”)。

(2)正确的操作顺序是 (填字母序号)。
(3)上述B步操作的目的是 。
(4)判断到达滴定终点的实验现象是 。
(5)上述A步操作之前,若先用待测溶液润洗锥形瓶,则对滴定结果的影响是 (填“偏大”或“偏小”或“无影响”)。
(6)若平行实验三次,记录的数据如下表
滴定次数 | 待测溶液的体积(/mL) | 标准NaOH溶液的体积 | |
滴定前读数(/mL) | 滴定后读数(/mL) | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
试计算待测盐酸的物质的量浓度(列出计算过程)。
(1)乙(2分) (2)BDCEAF(或ABDCEF)(2分)
(3)防止滴定管内壁附着的水将标准溶液稀释而带来误差(2分)
(4)溶液由无色变为浅红色,且半分钟内不褪色(2分)
(5)偏大(2分)(6)0.0800 mol·L-1(2分)
【解析】
试题分析:⑴碱式滴定管的下端为橡皮管(乙);
⑵滴定操作顺序为:取待测液(或放在装完标准液之后)、装标准液[润洗、装液、赶气泡、调液面、读数]、最后滴定读数,重复操作;
⑶用标准NaOH溶液润洗滴定管2~3次,能防止滴定管内壁附着的水将标准溶液稀释而带来误差;
⑷当溶液由无色变为浅红色(NaOH过量遇酚酞变红),且半分钟内不褪色可判断到达滴定终点;
⑸若先用待测溶液润洗锥形瓶,会使待测物的量偏多,测定结果偏大;
⑹三组标准NaOH溶液体积的平均值为20.00mL,则待测盐酸的物质的量浓度为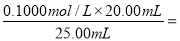 0.0800 mol·L-1。
0.0800 mol·L-1。
考点:考查酸碱中和滴定实验。


科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
在2L密闭容器中进行的反应2SO2(g)+O2(g) 2SO3(g),在10秒内反应物SO2的物质的量由1mol降到0.6mol,则反应速率ν(O2)为( )
2SO3(g),在10秒内反应物SO2的物质的量由1mol降到0.6mol,则反应速率ν(O2)为( )
A.0.02mol/(L·s) B.0.04mol/((L·s) C.0.01mol/((L·s) D.0.2mol/((L·s)
查看答案和解析>>
科目:高中化学 来源:2013-2014江西八一中学、洪都中学下学期期中考试高一化学试卷(解析版) 题型:选择题
同主族两种元素原子的核外电子数的差值可能是
A.6 B.12 C.26 D.30
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:选择题
常温下,0.1mol·L-1CH3COONa溶液中,微粒浓度间关系正确的是
A.c(Na+)=c(CH3COO-) >c(OH-)=c(H+)
B.c(OH-)=c(H+)+ c(CH3COOH)
C.c(Na+) + c(H+)= c(CH3COO-) +c(OH-)
D.c(CH3COOH) + c(CH3COO-) = c(Na+)+ c(H+)
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是
A.碳酸钙溶于醋酸:CaCO3 + 2H+ = Ca2++ CO2↑+H2O
B.苯酚钠溶液中通入少量的CO2: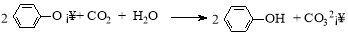
C.用铜做电极电解CuSO4溶液:2Cu2++2H2O 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
D.用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2+ +2OH-
CH3COO-+NH4++3NH3+2Ag↓+H2O
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高一下学期期末考试化学试卷(解析版) 题型:选择题
下列装置或操作能达到实验目的的是

A.蒸馏石油 B.除去甲烷中少量乙烯 C.验证化学能转变电能 D.制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省第二学期期中考试高一化学试卷(解析版) 题型:选择题
0.3 mol Cu与足量的稀HNO3完全反应时,被还原的HNO3的物质的量是
A.0.3 mol B.0.6mol C.0.4 mol D.0.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com