
| A、46g NO2和N2O4的混合气体中含有的原子数为3NA |
| B、标准状况下22.4L氢气中含有中子数为2NA |
| C、1L 浓度为1mol?L-1的醋酸溶液中含离子总数为2NA |
| D、1mol Mg与足量O2或N2反应生成MgO或Mg3N2均失去2NA个电子 |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
| A、煤的干馏和石油的分馏均属化学变化 |
| B、BaSO4 在医学上用作钡餐,所以Ba2+对人体无毒 |
| C、14C可用于文物的年代鉴定,14C与12C互为同素异形体 |
| D、葡萄糖注射液不能产生丁达尔现象,不属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
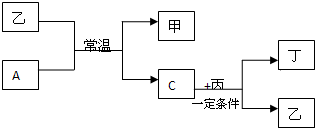
查看答案和解析>>
科目:高中化学 来源: 题型:
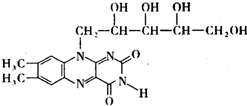 含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌.研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如图下列有关核黄素的说法中,正确的是( )
含工业染色剂“苏丹红一号”的有毒食品曾流入市场,引起人们的恐慌.研究表明:核黄素(即维生素B2)能缓解“苏丹红一号”的毒性,其结构如图下列有关核黄素的说法中,正确的是( )| A、核黄素属于分子晶体 |
| B、核黄素能发生银镜反应 |
| C、核黄素属于糖类 |
| D、核黄素不能被酸性高锰酸钾溶液氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3溶液中加过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-═BaCO3↓+2H2O+CO32- |
| B、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
| C、氯气溶于水:Cl2+H2O?2H++Cl-+ClO- |
| D、向NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、已知常温下,物质的量浓度相等的CH3COONa与CH3COOH混合液的pH<7,在此溶液中继续加CH3COONa至pH=7,测得此时c(Na+)=0.1 mol?Lˉ1,则此时溶液中存在:c(Na+)=c(CH3COOˉ)>c(CH3COOH)>c(H+)=c(OHˉ) |
| B、0.01 mol?Lˉ1的Na2HPO4溶液中存在如下的平衡:HPO42ˉ+H2O?H2PO4ˉ+OHˉ HPO42ˉ?H++PO43ˉ且溶液pH>7;加水稀释后溶液中HPO43ˉ、PO43ˉ、H+的浓度均减小 |
| C、常温下,pH=6的盐酸和PH=6的NH4Cl溶液,其中水电离出的c(H+)值分别是xmol?L-1、y mol?L-1,两者关系是x>y |
| D、已知25℃时AgCl的Ksp=1.8×10-10,AgI的Ksp=9.5×l0-17,若在5mL含有KCl和KI各为0.0l mol?L-1的溶液中,加入8mL0.01 mol?L-1AgNO3溶液,这时溶液中所含溶质的离子浓度大小关系为c(NO3-)>c(K+)>c(Ag+)>c(Cl-)>c(I-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、释热77 kJ/mol |
| B、释热55 kJ/mol |
| C、吸热77 kJ/mol |
| D、吸热55 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com