
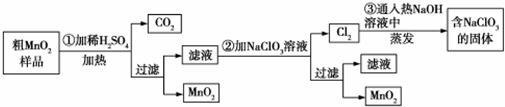
分析 粗MnO2(含有较多的MnO、MnCO3)样品中加入过量的稀硫酸,由于MnO2不溶于硫酸,则样品中的MnO和MnCO3分别和硫酸反应生成可溶性的MnSO4,过滤得滤液为硫酸锰溶液,加入NaClO3发生反应为:5Mn2++2ClO3-+4H2O=5MnO2+Cl2↑+8H+,再过滤得到滤液和二氧化锰固体,而氯气与热的氢氧化钠反应生成氯酸钠方程式为:3Cl2+6NaOH=NaClO3+NaCl+3H2O,
(1)二氧化锰有氧化性,在加热时浓盐酸能被MnO2氧化生成Cl2,据此答题;
(2)氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性;操作②中硫酸锰溶液,加入NaClO3发生氧化还原反应生成MnO2、Cl2,根据方程式转移电子数计算生成的氧化产物的物质的量;
(3)①二氧化锰在碱性条件下被氧气氧化可制取K2MnO4,为使二氧化锰能被充分氧化,工业上不断搅拌,使反应物与O2充分接触;
②电解K2MnO4的浓溶液时,生成高锰酸钾和氢气;
(4)根据反应MnO2+4HCl+2KI═MnCl2+I2+2KCl+2H2O,I2+2Na2S2O3═2NaI+Na2S4O6可得关系式MnO2~2Na2S2O3,根据Na2S2O3的物质的量可计算出二氧化锰的质量,进而确定该样品中MnO2含量.
解答 解:(1)二氧化锰有氧化性,在加热时浓盐酸能被MnO2氧化生成Cl2,所以不能用盐酸代替硫酸,
故答案为:否;浓盐酸能被MnO2氧化生成Cl2;
(2)操作②中硫酸锰溶液,加入NaClO3发生氧化还原反应生成MnO2、Cl2,反应的离子方程式为5Mn2++2ClO3-+4H2O=5MnO2+Cl2↑+8H+,ClO3-作氧化剂,MnO2作氧化产物,则氧化性:ClO3->MnO2;当NaClO3转移2mol电子时,消耗NaClO3为0.4mol,则生成MnO2为1mol;NaClO3在常温下与盐酸反应生成氯气,其反应的离子方程式为:ClO3-+5Cl-+6H+=3Cl2↑+3H2O;
故答案为:>;5Mn2++2ClO3-+4H2O=5MnO2+Cl2↑+8H+;1;
(3)①二氧化锰在碱性条件下被氧气氧化可制取K2MnO4,反应的方程式为2MnO2+4KOH+O2=2 K2MnO4+2H2O,为使二氧化锰能被充分氧化,工业上不断搅拌,使反应物与O2充分接触,
故答案为:2MnO2+4KOH+O2=2 K2MnO4+2H2O;使反应物与O2充分接触;
②电解K2MnO4的浓溶液时,生成高锰酸钾和氢气,电解的总反应方程式为2 K2MnO4+2H2O═KMnO4+2KOH+H2↑,
故答案为:2 K2MnO4+2H2O═KMnO4+2KOH+H2↑;
(4)根据反应MnO2+4HCl+2KI═MnCl2+I2+2KCl+2H2O,I2+2Na2S2O3═2NaI+Na2S4O6可得关系式MnO2~2Na2S2O3,根据题意可知Na2S2O3的物质的量为0.1000mol/L×0.001VL=0.0001Vmol,所以二氧化锰的质量为0.0001Vmol×87g/mol×$\frac{1}{2}$=0.00435Vg,则该样品中MnO2含量为$\frac{0.00435Vg}{ag}$×100%=$\frac{0.435V}{a}$%,
故答案为:$\frac{0.435V}{a}$.
点评 本题考查物质的分离与提纯方法的综合应用,题目难度中等,把握流程中发生的化学反应及原电池和电解池原理为解答的关键,注意掌握化学实验基本操作方法和根据关系式进行化学计算,试题侧重分析能力及推断能力的考查.


科目:高中化学 来源: 题型:选择题
| A. | ②③⑤ | B. | ①⑥ | C. | ①④⑤ | D. | 只有⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
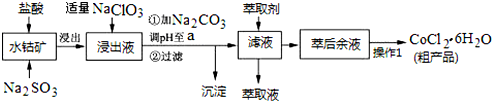
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuCl2 CH3COOH NaOH | B. | HCl H2SO3 NaHCO3 | ||
| C. | HF HCl CH3COONa | D. | NH4Cl HCl CH3COONa |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1,则H2燃烧热为241.8 kJ•mol-1 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,若将含0.6 mol H2SO4的稀硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| D. | 由BaSO4(s)+4C(s)═4CO(g)+BaS(s)△H1=+571.2kJ•mol-1①BaSO4(s)+2C(s)═2CO2(g)+BaS(s)△H2=+226.2kJ•mol-1②可得反应C(s)+CO2(g)═2CO(g) 的△H=+172.5kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C10H8和C6H8O3 | B. | C2H2和C6H6 | C. | C2H4和C3H6 | D. | CH4和C2H4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向FeSO4溶液中通入过量Cl2 | |
| B. | 向NaHCO3溶液中加入一定质量的Na2O2粉末 | |
| C. | 向NaI和NaBr混合溶液中通入过量Cl2 | |
| D. | 向NaOH溶液中加入过量AlCl3(SO4)3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com