
���� ����ƽ��״̬�Ľ�����ֻ��������أ������¶ȡ�ѹǿ�����������ݻ�������Ӧ������������ʼ������Թ�ϵ�йأ����뷴Ӧ���еķ����أ�
��˶��ڸ������µķ�Ӧ����ʼ̬��2 mol SO2��1 mol O2�Ļ�������2 mol������SO3�������ǵȼ۵ģ����յ����ƽ��״̬��ȫ��ͬ����ˣ�1���д�ӦΪc=2��
����2���г�ʼ̬������������̬���ʣ���ʱ��Ҫ����˼άת��������ʼ���ʵļ�����ת��Ϊ�൱��a=2��b=1���Ϳ��Դﵽ�����ƽ��״̬������a=0.5����b�T0.25����ʱ����������ʼ̬�IJ���ǡ�a=2-0.5=1.5����b=1-0.25=0.75���ɴ�SO3�ij�ʼ������c����ת��Ϊ��Ч��a=1.5��b=0.75���������ݸ÷�Ӧ����ʽ�Ļ�ѧ���������ƶ�֪c=1.5��
��3����Ҫ�����������Ϊ�ձ���ɣ���ʱ������ա������г�ʼ�ﶼת��Ϊ��Ӧ�������൱��2 mol SO2��1 mol O2�Ļ��������еij�ʼ��ת��Ϊ�����������൱��2 mol������SO3�������ܵó���ȷ���ۣ�����ͬʱ����a+c=2��2b+c=2������ϵʽ��
��� �⣺����ʼʱ2ĦSO2��1ĦO2Ϊ��״̬����������Ϊ��״̬���¶Ȳ��䣬�������ʱ��
���ݸı���ʼ�������������ֻҪͨ�����淴Ӧ�Ļ�ѧ�������Ȼ��㣨������ת�����ɷ�Ӧ����ʽ���ң���ͬһ�����ʵ����ʵ�����ԭƽ����ͬ���ɣ����÷���ʽ��⣺
��1��2SO2+O2?2SO3
��2mol 1mol 0
��0 0 cmol
���ݷ���ʽ��֪��2 mol SO3�൱��2 mol SO2��1 mol O2����c=2 mol��
�ʴ�Ϊ��c=2��
��2��2SO2+O2?2SO3
��2mol 1mol 0
��0.5mol bmol cmol
���У�0.5+c=2��b+$\frac{c}{2}$=1����֮�ã�b=0.25 mol��c=1.5 mol��
�ʴ�Ϊ��b=0.25��c=1.5��
��3��2SO2+O2?2SO3
��2mol 1mol 0
��a b c
��SO2��SO3�����ʵ���֮��Ϊ2 molʱ�����ܱ�֤��Ӧ��ʼSO2�����ʵ���Ϊ2mol����a+c=2mol����ʱҪ��O21mol����ô����b+0.5c=1mol��
���������������ʹƽ������˵ƽ����ȫ��ͬ���ʴ�Ϊ��a+c=2��2b+c=2��
���� �����ǶԿ��淴Ӧ�ͻ�ѧƽ��״̬�������Լ����������Ϣ����ѧ�����Լ����ڹ��ɳ���Ϊ��ѧ���⣬������ѧ���߽����ѧ�����˼ά�������ۺϿ��飮����ʱע���ڶ��£�T�������ݣ�V�������£���������ƽ����ϵ�в���ͬ�����ʵİٷֺ�����ȣ��������ʵ���Ũ�ȡ����ʵ���Ҳ�ֱ���ȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1����3����5����6�� | B�� | ��1����2����3����5�� | C�� | ��1����2����4����5�� | D�� | ȫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | s���ӵ�ԭ�ӹ���������εģ�2s���ӱ�1s�����������ҵ����Ʊ�1s����ɢ | |
| B�� | p���ӵ�ԭ�ӹ�����ǷĴ��εģ�ÿ��p�ܼ���3��ԭ�ӹ�����������ֱ������ͬ | |
| C�� | �������Ų���ͬһ�ܼ��IJ�ͬ������������ȵ���ռ��һ��������������������෴ | |
| D�� | ��һ��ԭ�ӹ������ֻ������2�����ӣ��������ǵ����������෴ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѹ�����ڰ��ĺϳ� | |
| B�� | ʵ�����г����ű���ʳ��ˮ�ķ�ʽ�ռ����� | |
| C�� | ����ˮƿ�������ݴ���Һ��ð�� | |
| D�� | ��˫��ˮ�м�������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
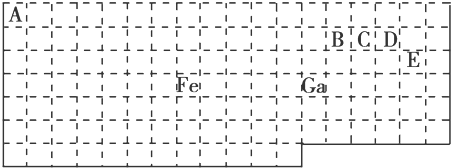
 ��ͼ��ʾ��ÿ����Ŵ������������е�һ�����ʣ�����ֱ���������������ʾ��ܷ�����ѧ��Ӧ������д�������У�a��Na2CO3��Һ b MgSO4��Һ c BaCl2��Һ dϡ���� e �� f Cu��NO3��2��Һ��
��ͼ��ʾ��ÿ����Ŵ������������е�һ�����ʣ�����ֱ���������������ʾ��ܷ�����ѧ��Ӧ������д�������У�a��Na2CO3��Һ b MgSO4��Һ c BaCl2��Һ dϡ���� e �� f Cu��NO3��2��Һ��| A�� | e | B�� | d | C�� | f | D�� | c |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��C��s��ʯī���TC��s�����ʯ����H=+1.9 kJ•mol-1����֪ʯī�Ƚ��ʯ���ȶ� | |
| B�� | ���������������������ֱ���ȫȼ�գ����߷ų����������� | |
| C�� | ��H+��aq��+OH-��aq���TH2O��l����H=-57.3 kJ•mol-1����֪��1 mol CH3COOH����Һ�뺬1 mol NaOH����Һ��ֻ�Ϸ�Ӧ���ų�����������57.3 kJ | |
| D�� | 2g H2��ȫȼ������Һ̬ˮ�ų�285.8 kJ������������ȼ�յ��Ȼ�ѧ����ʽΪ2H2��g��+O2��g���T2H2O��l����H=+571.6 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������a��b��c��d | B�� | ���ӵĻ�ԭ��Y2-��Z- | ||
| C�� | �⻯����ȶ���H2Y��HZ | D�� | Ԫ�صĽ����ԣ�W��X |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com