
分析 (1)在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中,根据化合价不交叉的原则,KClO3中+5价的氯元素降为0价,HCl中氯元素升为0价,氯化钾中的氯元素来自盐酸,所以KClO3是氧化剂、部分HCl是还原剂,氧化剂被还原、还原剂被氧化,据此分析解答;
(2)ClO2处理水时,发生反应,NaClO2→ClO2,+3价的氯元素化合价升高到+4价,NaClO2→NaCl,+3价的氯元素的化合价降低到-1价,由得失电子守恒分析;
(3)根据通入足量氯气,当反应恰好完全时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2失去的电子数相等,又溶液的体积相同,则浓度之比等于物质的量之比;向FeBr2 溶液中通入等物质的量的Cl2,先与亚铁离子反应,再与溴离子反应.
解答 解:(1)根据化合价不交叉的原则,在KClO3+6HCl=KCl+3Cl2↑+3H2O的反应中,KClO3中+5价的氯元素降为0价,该氯原子为被还原的氯原子,HCl中氯元素升为0价,该氯原子为被氧化的氯原子,氯化钾中的氯元素来自盐酸,则被氧化发生氧化反应的Cl为5,
所以KClO3是氧化剂、部分HCl是还原剂,氧化剂被还原、还原剂被氧化,被氧化和被还原的元素都是Cl元素,其质量之比等于其物质的量之比=5:1;
反应中转移5mol电子生成3mol氯气,则转移1mol电子时,产生标准状况下的Cl2为0.6mol,其体积为13.44 L;
故答案为:5:1;13.44;
(2)ClO2处理水时,发生反应,NaClO2→ClO2,+3价的氯元素化合价升高到+4价,NaClO2→NaCl,+3价的氯元素的化合价降低到-1价,由得失电子守恒可知,方程式为5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;生成4molClO2,转移电子4mol,生成0.2mol ClO2转移电子的物质的量为0.2mol;
故答案为:5NaClO2+4HCl=4ClO2↑+5NaCl+2H2O;0.2;
(3)因KI、Na2SO3、FeBr2溶液,分别通入足量氯气均发生氧化还原反应,且反应恰好完全时,三种溶液消耗氯气的物质的量相同,则KI、Na2SO3、FeBr2失去的电子数相等,
设KI、Na2SO3、FeBr2的物质的量分别为x、y、z,由失去的电子数相等可知,
x×(1-0)=y×(6-4)=z×(3-2)+z×2×(1-0),解得x:y:z=6:3:2;
向FeBr2 溶液中通入等物质的量的Cl2,先与亚铁离子反应,再与溴离子反应,其反应方程式为:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-;
故答案为:6:3:2;2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl-.
点评 本题考查了氧化还原反应,题目涉及氧化还原反应的计算、方程式的书写等,要求学生具有分析和解决问题的能力,明确元素化合价是解本题关键,题目难度中等.


 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③④⑤⑥⑦⑧ | B. | ④⑤⑧ | C. | ④⑤⑦⑧ | D. | ③④⑤⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
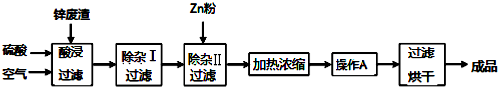
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Cu(OH)2 |
| 开始沉淀的 pH | 3.3 | 1.5 | 6.5 | 5.4 | 4.2 |
| 沉淀完全的 pH | 5.2 | 3.7 | 9.7 | 8.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、AlO2-、Cl-、SO42- | B. | H+、Ba2+、Cl-、NO3- | ||
| C. | Ca2+、Fe2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 轮船水线以下的船壳上装一定数量的锌块 | |
| B. | 红热的铁丝与冷水接触,表面形成蓝黑色保护层 | |
| C. | 纯锌与稀硫酸反应时,滴入少量CuSO4溶液后反应速率加快 | |
| D. | 烧过菜的铁锅加入清水放置,出现红棕色的锈斑 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 取a克混合物充分加热至质量不变,减重b克 | |
| B. | 取a克混合物与足量稀硝酸充分反应,加热、蒸干、灼烧至熔化,冷却得b克固体 | |
| C. | 取a克混合物与足量稀硫酸充分反应,逸出气体用碱石灰完全吸收,增重b克 | |
| D. | 取a克混合物与足量Ba(OH)2溶液充分反应,过滤、洗涤、烘干,得b克固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 我们使用合金是因为它比纯金属具有更优良的化学性质 | |
| B. | 钢化玻璃、有机玻璃、防弹玻璃均属于硅酸盐材料 | |
| C. | 高分子材料可能在特殊情况导电,如聚乙炔 | |
| D. | 可用作荧光灯内壁保护层的纳米氧化铝属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com