
【题目】下列物质:①H3O+ ②[Cu(NH3)4]2+ ③CH3COO- ④NH3 ⑤CH4中存在配位键的是
A. ①② B. ①③ C. ④⑤ D. ②④
【答案】A
【解析】
在物质或离子中中心原子含有空轨道,和含有孤电子对的原子或离子能形成配位键,①氢离子提供空轨道,氧原子提供孤电子对;②铜离子提供空轨道,氮原子提供孤电子对;③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对;④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;⑤CH4 分子中,碳原子与4个氢原子分别共用一对电子,形成4个C-H键,无空轨道,无孤电子对。
①H3O+中O提供孤电子对,H+提供空轨道,二者形成配位键,H3O+含有配位键;②Cu2+有空轨道,NH3中的氮原子上的孤电子对,可以形成配位键,[Cu(NH3)4]2+ 含有配位键;③CH3COO- 中碳和氧最外层有8个电子达到稳定结构,氢满足2电子稳定结构,无空轨道,无孤电子对,电子式为:![]() ,不含有配位键;④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;⑤甲烷中碳原子满足8电子稳定结构,氢原子满足2电子稳定结构,电子式为
,不含有配位键;④NH3为共价化合物,氮原子中最外层有8个电子达到稳定结构,分子中存在两个H-N键,氢满足2电子稳定结构,无空轨道;⑤甲烷中碳原子满足8电子稳定结构,氢原子满足2电子稳定结构,电子式为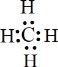 ,无空轨道,无孤电子对,CH4不含有配位键;答案选A。
,无空轨道,无孤电子对,CH4不含有配位键;答案选A。


科目:高中化学 来源: 题型:
【题目】已知NA为阿伏伽德罗常数的值.下列说法不正确的是 ( )
A. 1molCH4中含4NA个s﹣pσ键
B. 1molSiO2晶体中平均含有4NA个σ键
C. 12g石墨中平均含1.5NA个σ键
D. 12g金刚石中平均含有2NA个σ键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示。下列叙述中,正确的是( )
2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示。下列叙述中,正确的是( )
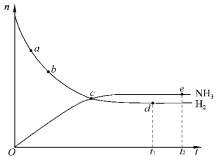
A. 点a的正反应速率比点b的小
B. 点c处正反应速率和逆反应速率相等
C. 点d (t1时刻) 和点 e (t2时刻) 处n(N2)相同
D. 在t2时刻,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医用麻醉药苄佐卡因E和食品防腐剂J的合成路线如下:
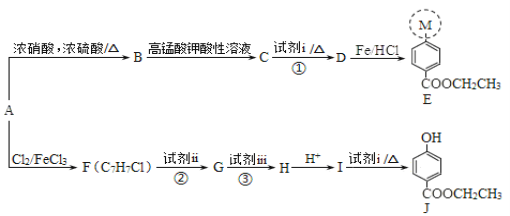
已知:I.M代表E分子结构中的一部分
II.![]()
请回答下列问题:
(1)A属于芳香烃,分子式为C7H8 ,其名称是_______,A到B的反应类型是______________________。
(2)E中所含含氧官能团的名称是_______,M的结构简式是__________。
(3)C能与NaHCO3溶液反应,则反应①的化学方程式是_____________。
(4)反应②、③中试剂ii和试剂iii依次是_______。(填序号)
a.高锰酸钾酸性溶液、氢氧化钠溶液
b.氢氧化钠溶液、高锰酸钾酸性溶液
(5)H的结构简式是_______。
(6)J有多种同分异构体,其中符合下列条件的同分异构体有______ 种,写出其中任一种同分异构体的结构简式:____。
a.为苯的二元取代物
b.遇到FeCl3溶液显紫色,能发生水解反应且能发生银镜反应
(7)以A为起始原料,选用必要的无机试剂合成涂改液的主要成分亚甲基环己烷(![]() ),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):_____________
),写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭 头上注明试剂和反应条件):_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
![]()
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、②的化学方程式________________、__________________。
(2)基态铜原子的核外电子排布式为____________,硫、氧元素相比,第一电离能较大的是______。
(3)反应①和②生成的气体分子的中心原子的杂化类型是______,分子的空间构型是______。
(4)C、Si为同一主族的元素,CO2和SiO2化学式相似,但结构和性质有很大不同。CO2中C与O原子间形成σ键和π键,SiO2中Si与O原子间不形成上述π键。从原子半径大小的角度分析,为何C、O原子间能形成,而Si、O原子间不能形成上述π键________________。
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密度为__________g·cm-3(用NA表示阿伏加德罗常数的数值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的H2和Cl2充分燃烧后,将反应生成的气体通入100mL1.0mol/L的NaOH溶液中,两者恰好完全反应,生成NaClO为0.01mol。则燃烧前H2和Cl2的物质的量之比为
A. 5:4 B. 4:5 C. 4:3 D. 3:4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com