
【题目】有两瓶无色溶液,一瓶为稀盐酸,一瓶为稀硝酸,能鉴别这两种溶液的合适试剂是( )
A.Na2CO3B.AgNO3C.NaOHD.BaCl2
科目:高中化学 来源: 题型:
【题目】下列物质:①H3O+ ②[Cu(NH3)4]2+ ③CH3COO- ④NH3 ⑤CH4中存在配位键的是
A. ①② B. ①③ C. ④⑤ D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个小烧杯里,加入20![]()
![]() 晶体,将小烧杯放在事先已滴有3~4滴水的玻璃片上。然后加入10
晶体,将小烧杯放在事先已滴有3~4滴水的玻璃片上。然后加入10![]()
![]() 晶体,并立即用玻璃棒快速搅拌。
晶体,并立即用玻璃棒快速搅拌。
(1)实验中观察到的现象有:玻璃片与小烧杯粘在一起;烧杯中产生__________的气体;反应混合物成糊状,出现糊状的原因是反应中有__________生成。
(2)写出有关反应的化学方程式__________。
(3)通过__________现象,说明该反应为__________(填“吸热”或“放热”)反应,这是由于反应物的总能量__________(填“小于”或“大于”)生成物的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示原电池装置,回答下列问题:
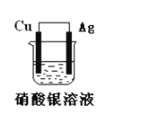
(1)此电池的负极是:______,正极的电极反应式是:________。
(2)该电池工作一段时间后,装置中出现的现象________,将银电极小心取出洗涤并晾干,经称量发现比原来增重了5.4g。则导线中通过的电子的物质的量为 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
试回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是______g,产生氢气的体积(标准状况)_________L。
(2)反应②中_________作氧化剂,___________是氧化产物。
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是____________。
(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)。___________
Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
(5)反应③中氧化产物与还原产物的物质的量之比为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水![]() 混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为
混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为![]() 。下列有关说法正确的是
。下列有关说法正确的是

A. 正极反应式:![]()
B. 放电过程中,![]() 向负极移动
向负极移动
C. 常温时,在正负极间接上电流表或检流计,指针发生偏转
D. 每转移0.1mol电子,理论上生成10.35gPb
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下图装置的叙述正确的是

A. 溶液中Na+向Fe极移动
B. 该装置中Pt为正极,电极反应为:O2 + 2H2O + 4e===4OH
C. 该装置中Fe为负极,电极反应为:Fe2e===Fe2+
D. 该原电池装置最终的产物是Fe(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学方程式或离子方程式,书写规范、正确的是(反应条件略)
A. 
B. 
C. 苯酚钠溶液中通入少量二氧化碳的离子方程式:![]() +H2O+CO2→
+H2O+CO2→![]() +HCO3-
+HCO3-
D. 乙酸与碳酸钠溶液反应的离子方程式:2H++CO32-=CO2↑+H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com