
【题目】已知:①Fe+H2SO4(稀)=FeSO4+H2↑
②Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O。
试回答下列问题:
(1)当反应①转移3摩尔电子时,消耗H2SO4的质量是______g,产生氢气的体积(标准状况)_________L。
(2)反应②中_________作氧化剂,___________是氧化产物。
(3)当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是____________。
(4)用单线桥法表示反应②电子转移的方向和数目(在化学方程式上标出)。___________
Cu+2H2SO4(浓)![]() CuSO4+2H2O+SO2↑
CuSO4+2H2O+SO2↑
(5)反应③中氧化产物与还原产物的物质的量之比为_________。
【答案】147 33.6 H2SO4(浓) CuSO4 0.5mol 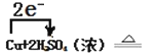 CuSO4+2H2O+SO2↑ 5:1
CuSO4+2H2O+SO2↑ 5:1
【解析】
(1)根据反应①Fe+H2SO4(稀)=FeSO4+H2↑可知每转移3mol电子,消耗硫酸3/2mol,生成氢气3/2mol;
(2)②Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑,根据氧化剂降得还,还原剂升失氧判断;
CuSO4+2H2O+SO2↑,根据氧化剂降得还,还原剂升失氧判断;
(3)根据②Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑,可以看出1molSO2生成,被还原硫酸1mol;
CuSO4+2H2O+SO2↑,可以看出1molSO2生成,被还原硫酸1mol;
(4)单线桥法表示箭头是还原剂指向氧化剂,写出转移电子数;
(5)根据还原剂升失氧,对应氧化产物;氧化剂降得还,对应还原产物,进行分析。
(1)Fe+H2SO4(稀)=FeSO4+H2↑,当反应①转移3摩尔电子时,消耗H2SO4的质量是3/2mol×98g/mol= 147g,产生氢气的体积(标准状况)3/2mol×22.4L/mol=33.6L;
答案:147 33.6
(2)Cu+2H2SO4(浓) ![]() CuSO4+2H2O+SO2↑,氧化剂化合价降低,所以浓硫酸为氧化剂,还原剂升失氧,对应氧化产物,硫酸铜为氧化产物;
CuSO4+2H2O+SO2↑,氧化剂化合价降低,所以浓硫酸为氧化剂,还原剂升失氧,对应氧化产物,硫酸铜为氧化产物;
答案:H2SO4(浓) CuSO4
(3)1mol SO2生成,就有1mol硫酸被还原,当反应②中生成11.2LSO2气体(标准状况下)时,被还原的H2SO4的物质的量是![]() =0.5mol;
=0.5mol;
答案:0.5mol
(4)箭头还原剂指向氧化剂,注明转移电子数: 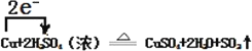 ;
;
答案:
(5)反应③KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O中氧化产物与还原产物均为氯气,根据还原剂升失氧,可知有5molCl-生成氯气,因此氧化产物为5/2mol,氧化剂降得还,1mol+5价氯生成氯气,因此还原产物为1/2mol,氧化产物与还原产物的物质的量之比为5:1。
答案:5:1


科目:高中化学 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示。下列叙述中,正确的是( )
2NH3(g)(正反应为放热反应),673K、30MPa下,n(NH3)和n(H2)随时间 t变化的关系如图所示。下列叙述中,正确的是( )
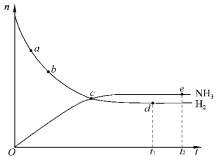
A. 点a的正反应速率比点b的小
B. 点c处正反应速率和逆反应速率相等
C. 点d (t1时刻) 和点 e (t2时刻) 处n(N2)相同
D. 在t2时刻,正反应速率大于逆反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,下列叙述不是可逆反应A(g)+3B(g) ![]() 2C(g)达到平衡的标志的是:①C的生成速率与C的分解速率相等;②单位时间内有a mol A生成的同时生成3a mol B;③A、B、C的浓度不再变化;④容积不变的密闭容器中混合气体的总压强不再变化;⑤混合气体的物质的量不再变化;⑥单位时间消耗a mol A,同时生成3a mol B;⑦A、B、C的分子数目之比为1∶3∶2。
2C(g)达到平衡的标志的是:①C的生成速率与C的分解速率相等;②单位时间内有a mol A生成的同时生成3a mol B;③A、B、C的浓度不再变化;④容积不变的密闭容器中混合气体的总压强不再变化;⑤混合气体的物质的量不再变化;⑥单位时间消耗a mol A,同时生成3a mol B;⑦A、B、C的分子数目之比为1∶3∶2。
A. ②⑤ B. ①③ C. ②⑦ D. ⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列五种物质:
A.食盐 B.食醋 C.苹果汁 D.葡萄糖 E.青霉素
请按下列要求填空(填序号,每空只填一个):
富含维生素C的是___;可直接进入血液,补充能量的是___;应用最广泛的抗生素之一的是___;食用过多会引起血压升高、肾脏受损的___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:CH3CH2CH2CH2OH→CH3CH2CH2CHO
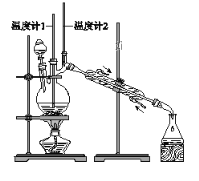
利用下图装置用正丁醇合成正丁醛。相关数据如下:
物质 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是( )
A. 为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B. 向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
C. 反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D. 当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:![]()
![]()
![]()
![]()
Ⅰ.冠心平F是降血脂、降胆固醇的药物,它的一条合成路线如下:
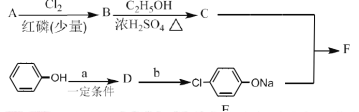
(1)A为一元羧酸,8.8gA与足量![]() 溶液反应生成2.24L
溶液反应生成2.24L![]() (标准状况),A的分子式为__________。
(标准状况),A的分子式为__________。
(2)写出符合A分子式的所有甲酸酯的结构简式:__________。
(3)B是氯代羧酸,其核磁共振谱有两个峰,写出![]() 的反应方程式:__________。
的反应方程式:__________。
(4)![]() 的反应类型为__________。
的反应类型为__________。
(5)写出A和F的结构简式:A.__________;F.__________。
(6)D的苯环上有两种氢,它所含官能团的名称为__________;写出a、b所代表的试剂:a.__________;b.__________。
Ⅱ.(7)有机物H的分子式为![]() ,可发生银镜反应,且具有酸性H有多种合成方法,在方框中写出由乙酸合成H的路线流程图(其他原料任选)______________________.
,可发生银镜反应,且具有酸性H有多种合成方法,在方框中写出由乙酸合成H的路线流程图(其他原料任选)______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人类必需的生命元素,在人体的生长发育过程中起着重要作用,实验小组进行碘单质的制备。
【查阅资料】碱性条件下,I2会发生歧化反应生成I-和IO3-,酸性条件下, I-和IO3-又会发生归中反应生成I2;碘在水中的溶解度为0.029g。
【碘的制取】以海带为原料,按照以下步骤进行实验。

(1)将海带灼烧成灰后再用水浸取,目的是_______________。
(2)步骤B发生的反应是“氧化”,这一操作中可供选用的试剂: ①Cl2;②Br2;③稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______(填编号),反应中I-转化为I2 的离子反应方程式为_______________。
(3)步骤C中使用的起到分离作用的仪器是_____________,使用该仪器时,第一步操作是_______________。
(4)有同学查资料后发现CCl4有毒,提议用乙醇代替,请判断该提议是否可行,原因是_______________。
【碘的分离】得到含I2的CCl4溶液后,利用右图装置进行碘的提取并回收溶剂。

(5)图中有两处明显错误,分别是①_________;②_________。
(6)对实验装置的错误改正之后进行分离操作。预期锥形瓶中得到无色的CCl4,实验结果锥形瓶中得到紫红色液体,请分析出现该实验结果的原因____________,为了保证实验成功,请提出改进方案:___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com