
| 浓硫酸 |
| 170℃ |
| 高温高压 |
| 催化剂 |
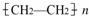
 ,
, .
.


科目:高中化学 来源: 题型:
| 选项 | 操作 | 现象 | 结论 |
| A | 将Cu片小心放入浓H2SO4中,加热 | 生成刺激性气味气体 | Cu与浓H2SO4反应生成SO2 |
| B | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| C | 向某溶液滴加硝酸酸化的BaCl2溶液 | 有白色沉淀生成 | 该溶液中一定含有SO42- |
| D | 某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
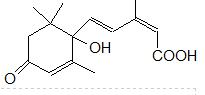 S-诱抗素的分子结构如图,下列关于该分子含有的官能团说法正确的是( )
S-诱抗素的分子结构如图,下列关于该分子含有的官能团说法正确的是( )| A、含有碳碳双键、羟基、羧基 |
| B、含有苯环、羟基、碳碳双键、羧基 |
| C、该物质能与烧碱溶液反应,但不能与纯碱溶液反应 |
| D、该物质为两性物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
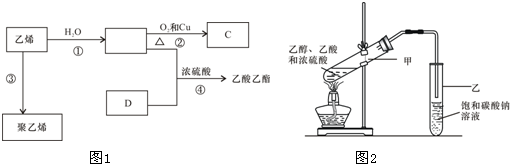
查看答案和解析>>
科目:高中化学 来源: 题型:
| /s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 S内的平均速率v(PCl3)=0.0032mol/(L?s) |
| B、保持其他条件不变,升高温度,平衡时c(PCl3=0.11)mol?L-1,该反应为放热反应 |
| C、相同温度下,起始时向容器中充入1.0 mol PC15、0.20 mol PC13和0.20 mo1 C12,达到平衡的v(正)>v(逆) |
| D、相同温度下,起始时向容器中充入2.0 mol PC13、2.0 mol C12,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com