
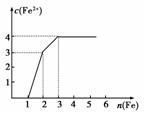
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
关于同一种元素的原子或离子,下列叙述正确的是
A.原子半径比阴离子半径小
B.原子半径比阴离子半径大
C.原子半径比阳离子半径小
D.带正电荷多的阳离子半径比带正电荷少的阳离子半径大
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.工业用电解熔融AlCl3的方法制金属铝
B.铅蓄电池工作时,正极反应为: PbO2 + 2e- + 4H+ + SO42- = PbSO4 + 2H2O
C.电解饱和食盐水时,用铁作阳极,Cl- 发生氧化反应
D.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,其与水的离子反应是4FeO42-+10H2O===4Fe(OH)3(胶体)+3O2↑+8OH-,工业上先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入一定量的KOH就可制得高铁酸钾。制备高铁酸钠的两种方法的主要反应原理如下:
湿法制备:2Fe(OH)3+3ClO-+4OH-===2FeO42-+3Cl-+5H2O;
干法制备:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑。
下列有关说法中错误的是
A.高铁酸钾与水反应时,水发生氧化反应
B.干法中每生成1 mol Na2FeO4共转移4 mol电子
C.湿法中每生成1 mol Na2FeO4共转移3 mol电子
D.K2FeO4处理水时,不仅能杀菌,并使悬浮杂质沉降
查看答案和解析>>
科目:高中化学 来源: 题型:
有关Al与NaOH溶液反应的说法中,正确的是
A.铝是还原剂,其还原产物是Al(OH)3
B.NaOH是氧化剂,其还原产物是H2
C.铝是还原剂,H2O和NaOH都是氧化剂
D.H2O是氧化剂,Al被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Fe3+、Fe2+、Al3+、 的稀溶液中加入足量Na2O2固体,充分作用后,再加入过量稀盐酸,完全反应,则离子数目没有变化的是
A.Fe3+、Al3+ B.Al3+ C.Fe2+、 D.Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
在Fe(OH)3胶体中,逐滴加入HI稀溶液,会出现一系列变化。
(1)先出现红色沉淀,原因是 。
(2)随后沉淀溶解,溶液呈黄色,此反应的离子方程式是 。
(3)最后溶液颜色加深,此反应的离子方程式是 。
(4)若用稀盐酸代替HI稀溶液,能出现上述哪些相同的变化现象(填写上面各题序号) 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com