
下列说法正确的是
A.工业用电解熔融AlCl3的方法制金属铝
B.铅蓄电池工作时,正极反应为: PbO2 + 2e- + 4H+ + SO42- = PbSO4 + 2H2O
C.电解饱和食盐水时,用铁作阳极,Cl- 发生氧化反应
D.电解精炼铜时,阳极泥中含有Zn、Fe、Ag、Au等金属
科目:高中化学 来源: 题型:
判断下列有关化学基本概念的依据正确的是
A 氧化还原反应:元素化合价是否变化
B 共价化合物:是否含有共价键
C 强弱电解质:溶液的导电能力大小
D 金属晶体:晶体是否能够导电
查看答案和解析>>
科目:高中化学 来源: 题型:
某有机物的结构简式为CH3—CH2—CH=CH—CHO,下列关于该有机物的说法不正确的是
A.该有机物可与新制Cu(OH)2悬浊液反应
B.该有机物不能发生水解反应
C.该有机物的核磁共振氢谱图有5个波峰
D.该有机物不能使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是用途广泛的金属材料,目前工业上主要用铝土矿(主要成分含氧化铝、氧化铁)来制取铝,其常见的过程如下:
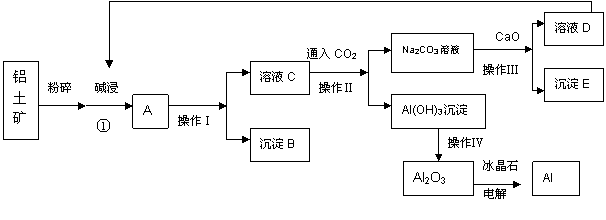 |
请回答下列问题:
(1)沉淀B的化学式为 ,溶液C中阴离子主要是 。
(2)操作Ⅰ是 (填操作名称)
(3)写出①过程中发生反应的离子方程式 。
(4)Al(OH)3沉淀必须进行洗涤才能通过操作Ⅳ获得纯净Al2O3,操作Ⅳ是 (填操作名称),简述洗涤沉淀的操作方法: 。
(5)生产过程中,除水、CaO和CO2可以循环使用外,还可循环使用的物质有 (填化学式)。
(6)电解Al2O3制取金属Al的阳极电极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是
A.打开汽水瓶有气泡从溶液中冒出
B.实验室用排饱和食盐水法收集氯气
C.合成氨工厂采用增大压强以提高原料的转化率
D.2NO2(g) N2O4(g)的平衡体系中, 加压缩小体积后颜色加深
N2O4(g)的平衡体系中, 加压缩小体积后颜色加深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关实验操作的说法正确的是
A.用10mL量筒量取8.10mL稀盐酸
B.用pH计测得某溶液的pH为2.2
C.用pH试纸测定溶液的pH时,需先用蒸馏水润湿试纸
D.可用25mL酸式滴定管量取20.00mL KMnO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上可利用“甲烷蒸气转化法生产氢气”,反应为:CH4(g)+H2O(g)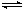 CO(g)+3H2(g)。
CO(g)+3H2(g)。
已知温度、压强和水碳比[n(H2O)/ n(CH4)]对甲烷平衡含量(%)的影响如下图1:
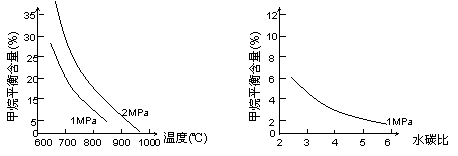 |
图1(水碳比为3) 图2(800℃)
(1)CH4(g)+H2O(g)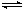 CO(g)+3H2(g)。的△H_______0 (填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。
CO(g)+3H2(g)。的△H_______0 (填“>”或“<”);若在恒温、恒压时,向该平衡体系中通入氦气平衡将 移动(填“向正应方向”、“向逆反应方向”或“不”)。
(2)温度对该反应的反应速率和平衡移动的影响是
。
(3)其他条件不变,请在图2中画出压强为2 MPa时,甲烷平衡含量(%)与水碳比之间关系曲线。(只要求画出大致的变化曲线)
(4)已知:在700℃,1MPa时,1mol CH4与1mol H2O在2L的密闭容器中反应,6分钟达到平衡,此时CH4的转化率为80%,求这6分钟H2的平均反应速率和该温度下反应的平衡常数是多少?(写出计算过程,结果保留小数点后一位数字。)
查看答案和解析>>
科目:高中化学 来源: 题型:
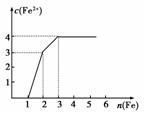
某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度与加入铁粉的物质的量之间的关系如图所示。则溶液中Fe(NO3)3、Cu(NO3)2、HNO3物质的量浓度之比为
A.1∶1∶1 B.1∶3∶1
C.3∶3∶8 D.1∶1∶4
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
H2可以催化还原NO以达到消除污染的目的:
(1)已知:①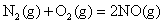
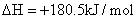
②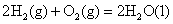

则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式为: ________________。
(2)一定条件下,在体积为2 L的容器中通入1 mol H2和l mol NO气体生成N2(g)和H2O(l),该反应达平衡时,容器内的压强是反应起始时的40%。保持其它条件不变,只往容器中再通入1 mol H2,计算反应再达新平衡时,化学平衡常数为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com