
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 0 | 50 | 120 | 232 | 290 | 310 |
分析 (1)先计算每个时间段的气体体积,然后根据相同条件下,气体体积与反应速率的关系判断反应速率大小,根据该反应与能量变化的关系判断速率变化原因;
(2)先求出气体的物质的量,然后计算盐酸变化的物质的量,利用速率公式计算即可;
(3)根据浓度、电解质的强弱对反应速率的影响判断.
解答 解:0~1 min、1~2 min、2~3 min、3~4 min、4~5min,各时间段的气体体积分别为:50 mL、70mL、112 mL、58 mL、20 mL,
(1)、相同通条件下,反应速率越大,相同时间内收集的气体越多;过计算得,反应速率最大的时间段是2~3 min,;原因是:该反应是放热反应,温度越高,反应速率越大,故答案为:先增大后减小;开始时因反应放热速率增大,随反应进行盐酸浓度降低,速率减小;
(2)2~3 min生成氢气的体积是112 mL,设需要盐酸的物质的量为xmol,
Zn+2HCl=ZnCl2 +H2 ↑
2 mol 22.4L
xmol 0.112L
则:x=0.01
所以v(HCl)=$\frac{\frac{△n}{V}}{△t}$=0.1mol/(L.min)
故答案为:0.1mol/(L.min);
(3)改变化学反应速率的方法有:改变溶液的浓度、改变溶液的温度、改变固体的表面积等;
A.加蒸馏水,溶液的体积增大,浓度降低,反应速率减小,但生成的气体的量不变,故A正确;
B.加NaNO3溶液中硝酸根离子与氢离子构成强氧化性体系,不生成氢气而生成氮的氧化物,所以生成氢气的量减少,故B错误;
C.加Na2CO3溶液,溶液的体积增大,盐酸的浓度降低,但盐酸和碳酸钠反应生成二氧化碳,氢气的量减小,故C错误;
D.CH3COONa溶液中的醋酸根离子与氢离子结合生成醋酸,溶液中的游离的氢离子的浓度减少,但提供氢离子的能力相同,所以生成氢气的量不变,故D正确
E.加CuSO4溶液,能形成铜锌原电池,加快反应速率,故E错误;
故选AD.
点评 本题主要考查化学反应速率的影响因素,题目难度中等,需要注意的是反应过程中浓度以及温度的变化,明确化学反应速率的概念及计算方法,注重基础知识的积累.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 第一电离能 | 电负性 | 晶格能 | 沸点 |
| O<N | Cl<F | NaCl<CaO | HF>HCl |
| 共价键 | H-Cl | O=O | H-O | Cl-Cl |
| 键能/kJ•mol-1 | 431 | 498 | 463 | 243 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 102 | 74 |
| 主要化合价 | +2 | +3 | +6、+4、-2 | -2 |
| A. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| B. | X和Y的金属性X<Y | |
| C. | 气态氰化物的稳定性H2Z<H2W | |
| D. | ZW3通常用单质Z与单质W反应制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
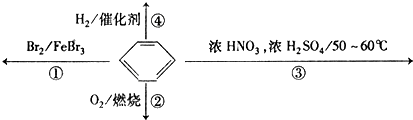
| A. | 反应①为取代反应,有机产物的密度比水小 | |
| B. | 反应②为氧化反应,反应现象是火焰明亮并带有较多的黑烟 | |
| C. | 反应③为取代反应,有机产物是一种烃 | |
| D. | 反应④1mol苯最多与3molH2发生加成反应,是因为苯分子含有三个碳酸双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分离液态空气制氮气 | |
| B. | 闪电将空气中的N2转化成NO | |
| C. | 工业上合成氮 | |
| D. | 豆科植物将空气中的N2转化为化合态氮 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 转化率(%) | 0.1MPa | 0.5MPa | 1.0MPa | 10MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能与碳酸钠反应产生气体 | B. | 能被酸性高锰酸钾氧化 | ||
| C. | 能发生酯化反应 | D. | 能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某铵态氮肥由W、X、Y、Z 4种短周期元素组成,其中W的原子半径最小.
某铵态氮肥由W、X、Y、Z 4种短周期元素组成,其中W的原子半径最小. ;
; ;
;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com