
A.S=100m/(a-m) B.S=100m2/c
C.S=100(m1-m2)/(b-c) D.S=100(m-m1)/(a-b)
解析:误选A、B、D的原因是,没有注意题干中标有加“.”的“不饱和”。误选A者,是由于错误的列式:m/(a-m)=S/100;误选B项者,是由于错误列式:m2/c=S/100;误选D项者,是由于错误列式(m-m1)/(a-b)=S/100。因而均是当作饱和溶液进行计算的。正确的思维过程是:当蒸发掉(b-c) g水时,可析出晶体(m1-m2)g,根据溶解度的概念列式:(m1-m2)/(b-c)=S/100〔或(m2-m1)/(c-b)=S/100〕即可求出答案。
思维敏捷的考生可以根据析晶后的溶液是饱和溶液,根据两次蒸发水的差值(b-c)和析出溶质的差值(m1-m2),便可在选项中找到答案C,因为选项中只有C中含有(b-c)。
答案:C


科目:高中化学 来源: 题型:阅读理解

| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| pH | 3.4 | 5.2 | 12.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
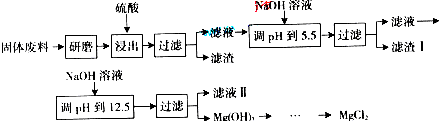
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| PH | 3.2 | 5.2 | 12.4 |

查看答案和解析>>
科目:高中化学 来源: 题型:
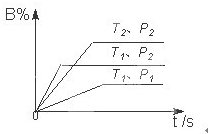 已知某可逆反应m A(g)+n B(g)?p C(g)△H,在密闭容器中进行,如图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )
已知某可逆反应m A(g)+n B(g)?p C(g)△H,在密闭容器中进行,如图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线.由曲线分析,下列判断正确的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
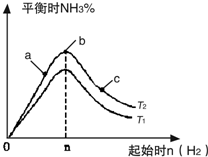 利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
利用N2和H2可以实现NH3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:| n |
| 3 |
| n |
| 3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com