
【题目】某大学实验室对煤矸石(主要含Al2O3、SiO2及Fe2O3)制备聚合氯化铝{[Al2(OH)nCl6-n]m}(1≤n≤5,m≤10),简称PAC,是一种新型、高效的絮凝剂和净水剂}。其工艺流程如下:

请回答下列问题:
(1)用浓盐酸配制20%的盐酸所需的玻璃仪器有______________________________。
(2)加20%的盐酸酸浸,有关反应的离子方程式为_____________________________。
(3)为了分析残渣2中铁元素的含量,某同学称取5.000g残渣2,先将其预处理使铁元素还原
Fe2+,并在容量瓶中配制成100mL溶液;然后移取25.00mL试样溶液,用1.000×10-2molL-1KMnO4标准溶液滴定,消耗标准溶液20.00mL.已知反应式为Fe2++MnO4-+H+—Fe3++Mn2++H2O(未配平).判断滴定终点的依据____ ;
残渣2中铁元素的质量分数为 _ .
(4)由澄清的PAC稀溶液获得聚合氯化铝固体,该实验操作是_______________,得到的PAC粗产品中可能含有的杂质离子是____________。
(5)从不引入杂质的角度来考虑,调节溶液pH的试剂可改为________(填字母)。
A.NaOH B.Al C.氨水 D.Al2O3
(6)若m=n=2,则生成PAC的化学方程式是 .
【答案】
(1)量筒、烧杯、玻璃棒
(2)Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O
(3)滴入最后一滴高锰酸钾溶液时,溶液出现紫红色且在半分钟内不变色;4.480%
(4)蒸发浓缩,冷却结晶;Ca2+(5)BD
(6)4AlCl3+2Ca(OH)2![]() [Al2(OH)2Cl4]2+2CaCl2
[Al2(OH)2Cl4]2+2CaCl2
【解析】
试题解析: (1)浓盐酸配20%的盐酸用到的仪器有:量筒、烧杯、玻璃棒,(2)氧化铝 氧化铁属于碱性氧化物,均能和强酸之间反应生成对应的盐和水,反应的方程式为:Al2O3+6H+=2Al3++3H2O、Fe2O3+6H+=2Fe3++3H2O,(3)氢氧化铝可以溶于强碱溶液中,但是氢氧化铁和氢氧化钠之间不反应,所以滤渣2是氢氧化铁,它可以和强酸之间反应得到三价铁盐,可以采用硫氰化钾检验三价铁的存在,取少量残渣2于小试管中,加入稀盐酸使其完全溶解,再加入KSCN溶液,溶液呈(血)红色;(4)从澄清的PAC稀溶液获得聚合氯化铝固体,可以采用蒸发浓缩,冷却结晶的方法,加入氢氧化钙调节溶液的pH过程中,引进的钙离子会混入PAC粗产品中,故答案为:蒸发浓缩,冷却结晶;Ca2+;(5)从不引入杂质角度去考虑,加入NaOH和氨水会引入钠离子和铵根离子,故选BD;(6)若m=n=2,氯化铝溶液与石灰水反应生成[Al2(OH)2Cl4]2 和CaCl2;反应为:4AlCl3+2Ca(OH)2 ![]() [Al2(OH)2Cl4]2+2 CaCl2
[Al2(OH)2Cl4]2+2 CaCl2


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示:下列描述正确的是

A.反应开始到10 s,用Z表示的反应速率为0.158 mol·(L·s)-1
B.反应开始到10 s,X的物质的量浓度减少了0.79 mol·L-1
C.反应开始到10 s时,Y的转化率为79.0%
D.反应的化学方程式为X(g)+Y(g)=Z(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一元弱酸(用HA表示)在水中的电离方程式是:HA![]() H++A-,回答下列问题:
H++A-,回答下列问题:
(1)向溶液中加入适量NaA固体,以上平衡将向___________(填“正”、“逆”)反应方向移动。
(2)若向溶液中加入适量NaCl溶液,以上平衡将向___________(填“正向”、“逆向”、或“不移动”)移动,溶液pH将___________中(填“增大”、“减小”或“不变”),溶液中![]() 比值___________(填“增大”、“减小”或“不变”).
比值___________(填“增大”、“减小”或“不变”).
(3)在25℃下,将a molL-1的氨水与0.01molL-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液呈中性,用含a的代数式表示NH3H2O的电离常数Kb=___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将Cl2通入氢氧化钾溶液中,反应后得到KCl、KClO、KClO3的混合溶液,经测定ClO﹣与ClO3-离子的物质的量之比是1:2,则Cl2与氢氧化钾反应时,被还原的氯元素和被氧化的氯元素的物质的量之比为( )
A. 2:3 B. 4:3 C. 10:3 D. 11:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将NH4NO3溶于水得无色溶液,为使该溶液中的c(NH4+)∶c(NO3-)=1∶1,可以采取的下列措施是
A.加入适量的HNO3,抑制NH4+水解 B.加入适量的氨水,使溶液的pH等于7
C.加入适量的NH4NO3(s) D.加入适量的NaOH,使溶液的pH等于7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比及产率等问题。
已知:CO(g)+H2O(g)![]() H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表:

试回答下列问题:
(1)上述反应平衡常数的表达式为_____________,正反应是___________反应(填“放热”或“吸热”)。
(2)某温度下,上述反应达到平衡后,保持容器体积不变升高温度,正反应速率_________(填“增大”“减小”或“不变”),容器内混合气体的压强______________(填“增大”“减小”或“不变”)。
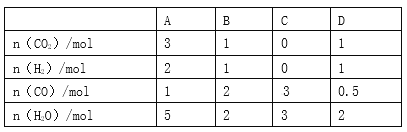
(3)830 ℃时,在恒容反应器中发生上述反应,按下表中的物质的量投入反应混合物,其中向正反应方向进行的有______________(选填字母)。
(4)830 ℃时,在2 L的密闭容器中加入4 mol CO(g)和6 mol H2O(g)达到平衡时,CO的转化率是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20世纪80年代后,人们发现和证实了一种新的含碳物质,它们是由一系列偶数个碳原子组成的分子,其中C60最具代表性。图中所示为n个C60连接而成的物质X 。下列有关说法不正确的是( )

A. X难溶于水,可以与氧气反应生成CO2
B. 该物质是一种新型的化合物
C. X是碳的一种同素异形体
D. X的摩尔质量为720ng·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类正确的是( )
酸 | 碱 | 盐 | |
A | H2SO4 | NaOH | BaCO3 |
B | H2S | K2CO3 | CuSO4 |
C | NaHSO4 | NaOH | CaCl2 |
D | HNO3 | KOH | Na2O |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com