
【题目】下列说法正确的是
A.从溶液中结晶出来的晶体都含结晶水
B.晶体失去结晶水一定是风化的结杲
C.风化与潮解是两个正好相反的过程
D.某饱和溶液冷却析出晶体后,该溶液仍是饱和溶液
 作业辅导系列答案
作业辅导系列答案 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】用下列装置制取NH3,并用AlCl3溶液吸收多余NH3制Al(OH)3,最后回收NH4Cl,能达到实验目的的是

A. 用装置甲制取NH3
B. 用装置乙吸收NH3制取Al(OH)3
C. 用装置丙分离Al(OH)3和NH4Cl溶液时,用玻璃棒不停的在漏斗内搅拌
D. 用装置丁蒸干NH4Cl溶液并灼烧制NH4Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100 mL甲气体经过下图实验的处理,结果得到酸性溶液,而几乎无气体剩余,则甲气体的组成为( )
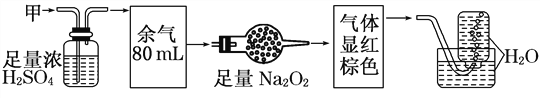
A. NH3、NO2、N2 B. NH3、NO、CO2
C. NH3、NO2、CO2 D. NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高炉炼铁中发生的基本反应之一如下:FeO(s)+CO(g)Fe(s)+CO2(g)(正反应是吸热反应),其平衡常数可表示为K= ![]() ,已知1100℃时K=0.263
,已知1100℃时K=0.263
(1)温度升高,化学平衡移动后达到新的平衡,高炉内CO2和CO的体积比值;平衡常数K值(选填“增大”“减小”或“不变”)
(2)1100℃时测得高炉中c(CO2)=0.025molL﹣1、c(CO)=0.1molL﹣1 , 在这种情况下,该反应是否处于化学平衡状态(选填“是”或“否”),此时,化学反应速率是v(正)v(逆)(选填“大于”“小于”或“等于”),其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电解池的叙述中不正确的是( )
A.与电源正极相连的是电解池的阴极
B.与电源负极相连的是电解池的阴极
C.在电解池的阳极发生氧化反应
D.电子从电源的负极沿导线流入电解池的阴极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】U、V、W、Y、Z是原子序数依次增大的短周期主族元素,U、Y在周期表中的相对位置如图1;U元素与氧元素能形成两种无色气体;W是地壳中含量最多的金属元素.
(1)元素Z在周期表中位于第族.我国首创以W组成的金属﹣海水﹣空气电池作为能源的新型海水标志灯,它以海水为电解质溶液,靠空气中的氧气使W组成的金属不断氧化而产生电流.只要把灯放入海水中数分钟,就会发出耀眼的白光.则该电源负极反应为 .
(2)YO2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VO,有关反应的离子方程式为 , 由此可知YO2和VO还原性较强的是(写化学式) .
(3)V的最简单气态氢化物甲的水溶液显碱性.①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为 .
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变如表中反应条件x,该平衡体系中随x递增y递增的是(选填序号).
选项 | a | b | c | d |
x | 温度 | 温度 | 加入H2的物质的量 | 加入甲的物质的量 |
y | 混合气体的平均相对分子质量 | 平衡常数K | 混合气体的密度 | 达平衡时的甲的转化率 |
③向含4molV 的最高价含氧酸的稀溶液中,逐渐加入Fe粉至过量.假设生成的气体只有一种,请在图2坐标系中画出n(Fe2+)随n(Fe)变化的示意图 .
(4)相同温度下,等体积、物质的量浓度都为0.1mol/L的KZ和CH3COOK溶液的两种溶液中,离子总数相比较 .
A.前者多
B.一样多
C.后者多
D.无法判断.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识回答问题:
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2═6SO2+Fe3O4 , 氧化产物为 , 若有3molFeS2参加反应,转移mol电子.
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为(用离子方程表示)
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+ , 并有气体逸出,请写出相应的离子方程式:
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL5molL﹣1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+ , 则参加反应的铁粉的质量为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com