
【题目】据报道,科学家已经研制出世界上最薄的材料——碳膜片,其厚度只有一根头发的二十万分之一。如图所示,这种碳膜片形状如蜂巢,是由碳原子构成的六边形单元向外延展而成,下列有关碳膜片的说法中,正确的是( )
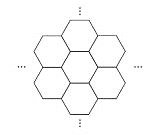
A. 碳膜片属于一种新型的化合物
B. 碳膜片与石墨的结构相同
C. 碳膜片与C60互为同素异形体
D. 碳膜片在氧气中完全燃烧的产物和碳在氧气中完全燃烧的产物不同
科目:高中化学 来源: 题型:
【题目】某废液中含有大量的K+、Cl-、Br-,还有少量的Ca2+、Mg2+、SO42-。某研究性学习小组利用这种废液来制取较纯净的氯化钾晶体及液溴(Br2常温下是深红棕色液体),设计了如下流程图:
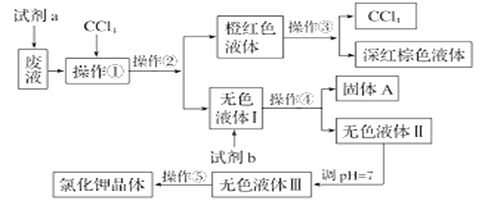
请根据流程图,回答相关问题:
(1)若试剂a为H2O2溶液(H+),已知氧化性:H2O2>Br2
①写出废液中的某阴离子和a发生反应的离子方程式为:__________________________;
②每消耗0.2mol H2O2,反应转移的电子为______mol;
(2)为了除去无色液体I中的Ca2+、Mg2+、SO42-,试剂b可选择:KOH、BaCl2、K2CO3溶液,其添加顺序不正确的是(_______)
A、KOH、BaCl2、K2CO3 B、BaCl2、KOH、K2CO3
C、BaCl2、K2CO3 、KOH D、KOH、K2CO3 、BaCl2
(3)用盐酸调pH=7(中性)是为了除去杂质离子___和___,以提高氯化钾晶体的纯度;
(4)操作①②③④⑤对应的名称分别是:____、分液、_____、过滤、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素是造成水体富营养化的主要原因,在水中常以氨氮或NO3形式存在。
(1)在pH为4~6时,用H2在Pd-Cu催化下将NO3-还原为N2可消除水中NO3。该反应的离子方程式为____。若用H2和CO2的混合气体代替H2,NO3-去除效果更好,其原因是____。
(2)NaClO氧化可除去氨氮,反应机理如图1所示(其中H2O和NaCl略去),实验测得相同条件下,相同反应时间,pH与氨氮的去除率关系如图2所示,温度与氨氮去除率关系如图3所示。



图1 图2 图3
①NaClO氧化NH3的总反应的化学方程式为____。
②如图2所示,在pH>9时,pH越大去除率越小,其原因是____。
③如图3所示,温度低于15℃时,温度越低去除率越低其原因是____。当温度高于25℃时,温度越高去除率也越低,其原因是____。
(3)用电化学法可去除废水中的氨氮。在含NH4+的废水中加入氯化钠,用惰性电极电解。反应装置如图4所示,则电解时,a极的电极反应式为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d四种元素在周期表中的位置如下图,则下列说法正确的是

A. a与b之间容易形成离子化合物
B. 若b的单质可作半导体材料,则c的单质不可能为半导体材料
C. 若b的单质与H2易化合,则c的单质与H2更易化合
D. 若b的最高价氧化物对应水化物为H2bO4,则a的氢化物的化学式为aH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。请回答下列问题:
(1)钴在元素周期表中的位置是___________,其基态原子的价电子排布图为___________。
(2)FeCO3是菱铁矿的主要成分,其中C原子的杂化方式为________;分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π![]() ),则CO32-中的大π键应表示为________。
),则CO32-中的大π键应表示为________。
(3)已知Fe2+半径为61pm,Co2+半径为65pm,在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3受热分解温度低于CoCO3,其原因可能是______。
(4)Co(NH3)5Cl3是钴的一种配合物,向含0.01mol该配合物的溶液中加入足量AgNO3溶液,生成白色沉淀2.87g。则该配合物的配位数为_____。
(5)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构(如图所示),则该晶体中与铁原子距离最近的铁原子数目为___________;若该晶胞参数为a pm,则该晶体的密度为___________g·cm-3(阿伏加德罗常数的值用NA表示)。
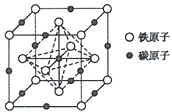
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求答题
(一)现有下列七种物质:①铝 ②蔗糖 ③CO2 ④H2SO4 ⑤Ba(OH)2 ⑥红褐色的氢氧化铁胶体 ⑦HCl ⑧冰水混合物 ⑨碳酸钙 ⑩CuSO4·5H2O。
(1)上述物质中属于电解质的有__________(填序号)。
(2)向⑥的溶液中逐渐滴加⑦的溶液,看到的现象是________________________。
(3)上述物质中有两种物质在水溶液中发生反应,其离子方程式为:H++OH-=H2O,则该反应的化学方程式为______________________________。
(二)(1)某气态氧化物化学式为RO2,在标准状况下,1.28 g该氧化物的体积是448 mL,则氧化物的摩尔质量为_______,R的相对原子质量为__________。
(2)在标准状况下,w L氮气含有x个N2分子,则阿伏加德罗常数为____________(用w,x表示)。
(3)过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4等杂质,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的BaCl2溶液;②加入稍过量的NaOH溶液;③加入稍过量的Na2CO3溶液;④滴入稀盐酸至无气泡产生;⑤过滤。正确的操作顺序是________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取碘水四份于试管中,编号为Ⅰ、Ⅱ、Ⅲ、Ⅳ,分别加入汽油、![]() 、酒精、NaCl溶液,振荡后静置,现象正确的是
、酒精、NaCl溶液,振荡后静置,现象正确的是![]()
![]()
A.Ⅰ中溶液分层,下层呈紫红色B.Ⅱ中溶液分层,下层呈紫红色
C.Ⅲ中溶液分层,下层呈黄褐色D.Ⅳ中溶液不分层,溶液由黄褐色变成黄绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出方程式:实验室制乙炔__________________;
(2)![]() 该有机物共面的原子最多有_____个,与溴发生加成反应的产物最多有_______种
该有机物共面的原子最多有_____个,与溴发生加成反应的产物最多有_______种
(3)有甲、乙两种物质:

由甲转化为乙需经下列过程(已省略去各步反应的无关产物)
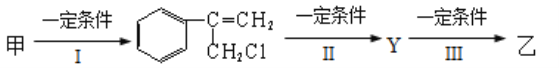
①反应I的反应类型是__________________,
②反应II的条件是_________________________________,
③反应III的化学方程式为______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据Mg能在CO2中燃烧,某兴趣小组推测Na应该也能在CO2中燃烧,且固体产物可能为C、Na2O和Na2CO3中的两种或三种。该小组用如下图装置进行了实验探究。已知PdCl2能被CO还原得到黑色的Pd。
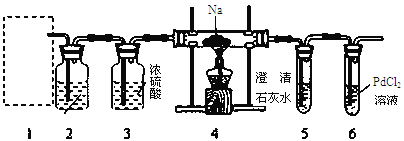
回答下列问题:
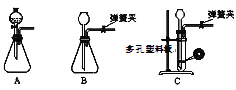
(1)为了使反应随开随用,随关随停,上图虚线方框内应选用____装置(填下图字母代号),如何检验所选装置的气密性_____。
(2)装置2中所盛试剂为_______。
A.NaOH溶液 B.饱和NaHCO3溶液
C.饱和Na2CO3溶液 D.饱和NaCl溶液
(3)检测装置的气密性完好并装好药品后,在点燃酒精灯前应先进行装置1中的反应操作,待观察到_____现象时,再点燃酒精灯,这步操作的目的是________。
(4)由实验现象和进一步的探究得出反应机理。
A.装置6中有黑色沉淀生成;
B.取反应后直玻管中的固体物质23.0g溶于足量的水中,无气泡产生且得到澄清的溶液;将溶液加水稀释配成250 mL的溶液;
C.取25.00ml步骤B的溶液,滴加足量BaCl2溶液,将生成的白色沉淀过滤、洗涤、干燥,称量得固体质量为1.97g。
①步骤C中不溶物干燥前必须经过洗涤,如何检验该沉淀是否洗涤干净____。
②该探究得出钠与二氧化碳反应的化学方程式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com