
����Ŀ����(N2H4)��һ��Ӧ�ù㷺�Ļ���ԭ�ϡ���ҵ���Ⱥϳɰ�����N2(g)+3H2(g)![]() 2NH3(g)��H��0���ٽ�һ���Ʊ��¡����������գ�
2NH3(g)��H��0���ٽ�һ���Ʊ��¡����������գ�
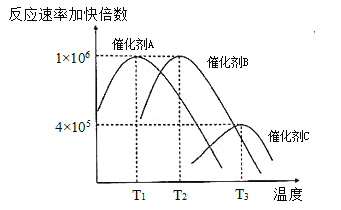
��1���ϳɰ���Ҫѡ����ʵĴ������ֱ�ѡ��A��B��C���ִ����������飬���ý����ͼ��ʾ(����������ͬ)��������������ѡ��Ĵ�����__(����A������B������C��)�������ǣ�__��
��2��һ�������£������ܱ������н��еĺϳɰ���Ӧ��ƽ���������������ʱ����ͬʱѹ������������������¶ȴ���ƽ�����ԭƽ����ȣ��뽫�й��������ı仯����������±���(����������������С��������ȷ����)
��Ӧ���� | ƽ�ⳣ��K | |
�仯��� | ____ | ____ |
��3��ͨ���Ѳ�1molij��ѧ�������յ��������ɸû�ѧ���ļ��ܡ���֪���ֻ�ѧ���ļ������£�
��ѧ�� | N��H | N��N | O==O | N��N | O��H |
����(kJ/mol) | 386 | 167 | 498 | 946 | 460 |
�������۷ɴ��ij������������(N2H4����̬)Ϊȼ�ϣ�����������(��̬)��ȼ�գ�����N2(��̬)��H2O(Һ̬)���÷�Ӧ���Ȼ�ѧ����ʽΪ��____��
��4������Ҫ�����������ʺ����ᡣ��ʮ�������ڼ䣬Ԥ���ҹ��ϳɰ�����������������������ͼ�Dz�ͬ�¶ȺͲ�ͬѹǿ�£���Ӧ�ﵽƽ��������NH3����(���%)�ı仯�������֪��ʼʱn(N2)��n(H2)=1:3���ж�pl��p2ѹǿ�Ĵ�С��ϵ��pl___p2(ѡ��������������������=��)��
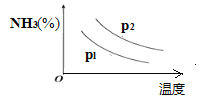
���𰸡�A �ڽϵ��¶��¾߱��ϸߵĴ����ԣ�һ����ɽ�Լ��Դ����һ������������ڷ�Ӧ��ת�� ���� ��С N2H4(g)+O2(g)��N2(g)+2H2O(l) ��H=-577kJ/mol ��pl��p2
��������
(1)����ͼ�������֪������A�ķ�Ӧ���ʼӿ�ı������¶ȵͣ�
(2)������������ʱ����ͬʱѹ��������������൱������ѹǿ�������¶ȴ���ƽ���N2(g)+3H2(g)2NH3(g) ��H��0����ӦΪ���������С�ķ��ȷ�Ӧ������ѹǿƽ�������ƶ��������¶�ƽ�������ƶ����ݴ˷������
(3)��д����ѧ����ʽN2H4+O2�TN2+2H2O��Ȼ������ʱ�=��Ӧ����ܼ���-��������ܼ��ܼ����ʱ䣬��д�Ȼ�ѧ����ʽ��
(4)���ݷ�Ӧ�ķ���ʽ���ƽ���ƶ���ԭ�������жϡ�
(1)�ϳɰ���Ҫѡ����ʵĴ������ֱ�ѡ��A��B��C���ִ����������飬���д���A�ڽϵ��¶��¾߱��ϸߵĴ����ԣ�һ����ɽ�Լ��Դ����һ������������ڷ�Ӧ��ת�����ʴ�Ϊ��A���ڽϵ��¶��¾߱��ϸߵĴ����ԣ�һ����ɽ�Լ��Դ����һ������������ڷ�Ӧ��ת����
(2)һ�������£������ܱ������н��еĺϳɰ���Ӧ��ƽ���������������ʱ����ͬʱѹ������������������¶ȴ���ƽ�����ԭƽ����ȣ���Ӧ�������÷�ӦΪ���ȷ�Ӧ��ƽ�ⳣ��ֻ���¶��йأ��¶����ߣ�ƽ�������ƶ���ƽ�ⳣ����С���ʴ�Ϊ������С��
(3)1molN2H4�����к�4molN-H����1molN-N����N2H4ȼ�յĻ�ѧ����ʽΪN2H4(g)+O2(g)�TN2(g)+2H2O(g)����H=��Ӧ����ܼ���-��������ܼ���=167 kJmol-1+386 kJmol-1��4+498 kJmol-1-946 kJmol-1-460 kJmol-1��4=-577 kJmol-1��N2H4ȼ�յ��Ȼ�ѧ����ʽΪN2H4(g)+O2(g)�TN2(g)+2H2O(g)��H=-577 kJmol-1���ʴ�Ϊ��N2H4(g)+O2(g)�TN2(g)+2H2O(g) ��H=-577 kJmol-1��
(4)�ϳɰ�Ϊ���������С�ķ�Ӧ��ѹǿԽ�����ĺ���Խ�ߣ�����ͼ���֪���¶���ͬʱp2�����°����ĺ����ϸߣ��� pl��p2ѹǿ�Ĵ�С��ϵΪ pl��p2���ʴ�Ϊ��pl��p2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���Ƚ���ǰ�߸��ڣ�����ڻ�ǿ�ڣ����ߵ���
A. CCl4��SiCl4���۵�
B. ���ǻ�����ȩ��![]() �������ǻ�����ȩ��
�������ǻ�����ȩ��![]() ���ķе�
���ķе�
C. I2��ˮ�е��ܽ�Ⱥ�I2��CCl4��Һ�е��ܽ��
D. H2SO3��H2SO4������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ǹ�ҵ�����в���ȱ�ٵ�һ�ֽ�������ش��������⣺
��1��FeԪ����Ԫ�����ڱ��е�λ����__��
��2��Fe����������������ͬ�������壬�侧���ṹ��ͼ��ʾ��
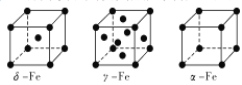
�����������־��徧������ԭ�ӵ���λ��֮��Ϊ__����������ʵ��ӵ��___��ԭ�ӡ�
����Feԭ�Ӱ뾶Ϊrpm��NA��ʾ�����ӵ�������ֵ������-Fe���ʵ��ܶ�Ϊ___g/cm3(�г���ʽ����)��
��3�����Ȼ����ڳ�����Ϊ����.�۵�Ϊ282�棬�е�Ϊ315�棬��300������������������ˮ��Ҳ���������ѡ���ͪ���л��ܼ����ݴ��ж����Ȼ����ľ�������Ϊ___��
��4���Ȼ�����Һ���ڼ���ʳ���㾫������������ʱ����������ɫ�����������ӽṹ��ͼ��ʾ��
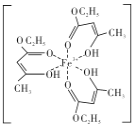
�ٴ��������̼ԭ�ӵ��ӻ����������___��
�ڴ��������к��еĻ�ѧ����___(����ĸ����)��
A.���Ӽ� B.������ C.���Լ� D.�Ǽ��Լ�
E.��� F.��� G.���� H.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£������������Ϊ0.5 L�ĺ����ܱ������з�����Ӧ��CO(g)+Cl2(g)![]() COCl2(g)�������������з�Ӧ��5 minʱ�ﵽƽ��״̬��
COCl2(g)�������������з�Ӧ��5 minʱ�ﵽƽ��״̬��
������� | �¶�/�� | ��ʼ���ʵ���/mol | ƽ�����ʵ���/mol | ||
CO | Cl2 | COCl2 | COCl2 | ||
�� | 500 | 1.0 | 1.0 | 0 | 0.8 |
�� | 500 | 1.0 | a | 0 | 0.5 |
�� | 600 | 0.5 | 0.5 | 0.5 | 0.7 |
����˵������ȷ����
A. ��������ǰ5 min��ƽ����Ӧ����v(CO)=0.16 mol��L-1��min-1
B. �÷�Ӧ����ӦΪ���ȷ�Ӧ
C. ����������ʼʱCl2�����ʵ���Ϊ0.55 mol
D. ����ʼʱ�����������CO0.8mol��Cl20.8mol���ﵽƽ��ʱCOת���ʴ���80%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����H2S��CO2�ڸ����·�����Ӧ��H2S(g)+CO2(g)![]() COS(g) +H2O(g)����610 Kʱ����0.10molCO2��0.40molH2S����2.5L�Ŀո�ƿ�У���Ӧƽ���ˮ���������ʵ�������Ϊ0.02����H2S��ƽ��ת����Ϊ____%����Ӧƽ�ⳣ��K=____������С�������λ����
COS(g) +H2O(g)����610 Kʱ����0.10molCO2��0.40molH2S����2.5L�Ŀո�ƿ�У���Ӧƽ���ˮ���������ʵ�������Ϊ0.02����H2S��ƽ��ת����Ϊ____%����Ӧƽ�ⳣ��K=____������С�������λ����
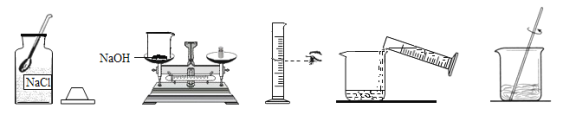
��ijѧ����0.200mol/L�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����
��������ˮϴ�Ӽ�ʽ�ζ��ܣ���ע��NaOH��Һ����0���̶�������
�ڹ̶��õζ��ܲ�ʹ�ζ��ܼ������Һ��
�۵���Һ������0������0���̶������£������µζ���Һ�����
����ȡ20.00mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ
���ñ�Һ�ζ����յ㣬���µζ���Һ�����
��ش�
��1�����ϲ����д������____�����ţ���
��2���ñ�NaOH��Һ�ζ�ʱ��Ӧ����NaOH��Һע��___��(��ͼ��ѡ����������������)��

��3�����в���������ʵ����ƫ����ǣ�____�����ţ���
A������ƿװҺǰ��������������ˮ
B���ζ�ǰ���ζ��ܼ��������ݣ��ζ���������
C���ζ��յ㸩�Ӷ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������80 g��������Ϊ10%������������Һ����ͼ�����Ƹ�����������Һ��ʵ�����ʾ��ͼ���ش��������⣺
��1�����㣺��Ҫ�������ƹ���___g��ˮ____mL��ˮ���ܶ���1.0g/cm3�ƣ���
��2����������������ƽ��ȡ�������ƹ��壬�ù��Ϊ____���10mL������50mL����100mL��������Ͳȡ����Ҫ��ˮ������ʢ���������Ƶ��ձ��С�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO���黯��ӦΪ��CO(g)+3H2(g)=CH4(g)+H2O(l)����ͼ��ʹ��ij�ִ���ʱת�������е������仯����������ʡ�ԣ������в���ڷ�Ӧ����������
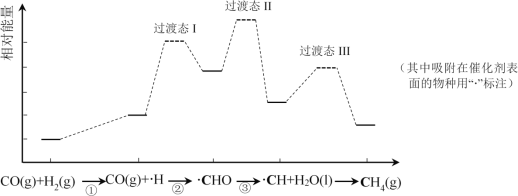
����˵������ȷ���ǣ� ��
A.�����ֻ�зǼ��Լ�����
B.���������������ԭ��������������
C.�������Ҫ��������
D.ʹ�øô���������Ч���CO��ƽ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijѧ��̽��0.25mol/L Al2( SO4)3��Һ��0.5mol/L Na2CO3��Һ�ķ�Ӧ��ʵ�����£�

���з�������ȷ����
A. ʵ��I�У���ɫ����a��Al(OH)3
B. ʵ��2�У���ɫ����b����CO32-
C. ʵ��l��2�У���ɫ�����ɷֲ�ͬ��ԭ�����Ϻ���Һ��pH��
D. �����ɫ����a��b���ϴ�Ӹɾ��������������ữ��BaCl2��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����н��Ͷ�Ӧ��ʵ�����ӷ���ʽ��ȷ����
A.FeSO4��Һ�еμ�NaOH��Һ������һ��ʱ���Fe2++2OHһ=Fe(OH)2��
B.Ư����Һ������H++ClO-=HC1O
C.AgCl����Һ����Na2S��Һ��2Ag++S2-=Ag2S��
D.K2 CrO4��Һ����������Һ��2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com