
| A、一定有乙烯 |
| B、一定没有乙烯 |
| C、一定没有甲烷 |
| D、一定没有乙烷 |
| 3.6g |
| 18g/mol |
| 3.6g |
| 18g/mol |


科目:高中化学 来源: 题型:
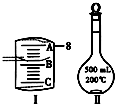 实验室要用Na2CO3?10H2O晶体配制500mL 0.1mol?L-1 Na2CO3溶液,回答下列问题:
实验室要用Na2CO3?10H2O晶体配制500mL 0.1mol?L-1 Na2CO3溶液,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16 g |
| B、32 g |
| C、64 g?mol-1 |
| D、32 g?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
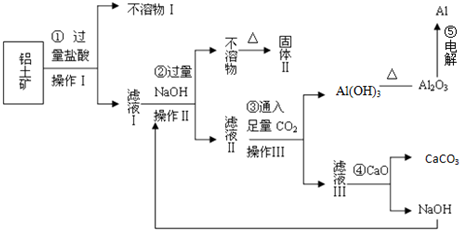
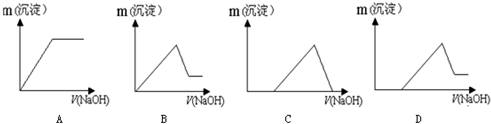
查看答案和解析>>
科目:高中化学 来源: 题型:
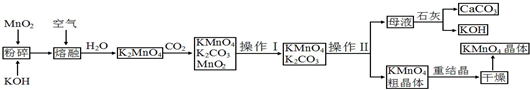
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进入煤矿井时,用火把照明 |
| B、在开阔广场燃放烟花爆竹 |
| C、用点燃的火柴检验液化气钢瓶是否漏气 |
| D、进入下水道时,应用蜡烛照明 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
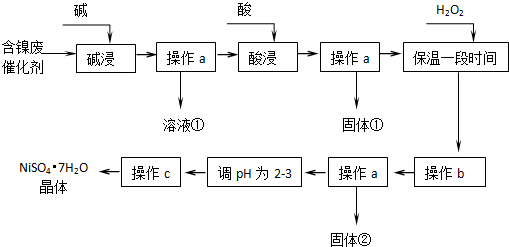
| 沉淀物 | 开始沉淀 | 完全沉淀 |
| Al(OH)3 | 3.8 | 5.2 |
| Fe(OH)3 | 2.7 | 3.2 |
| Fe(OH)2 | 7.6 | 9.7 |
| Ni(OH)2 | 7.1 | 9.2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com