
【题目】已知4P(红磷,s)![]() P4(白磷,s)△H=+17kJ·mol-l,下列推论正确的是
P4(白磷,s)△H=+17kJ·mol-l,下列推论正确的是
A.当1mol白磷转变成红磷时放出17kJ热量
B.当4g红磷转变成白磷时吸收17kJ热量
C.正反应是一个放热反应
D.白磷热稳定性比红磷大
科目:高中化学 来源: 题型:
【题目】某科研小组模拟的“人工树叶”电化学装置如图所示,该装置能将H2O和CO2转化为糖类(C6H12O6)和O2,X、Y是特殊催化剂型电极。已知装置的电流效率等于生成产品所需的电子数与电路中通过的总电子数之比。下列说法不正确的是( )

A.该装置中Y电极发生氧化反应
B.X电极的电极反应式为6CO2+24e-+24H+=C6H12O6+6H2O
C.理论上,每生成22.4LCO2必有4molH+由Y极区向X极区迁移
D.当电路中通过3mol电子时生成18gC6H12O6,则该装置的电流效率为80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氯苯的废水可通过加入适量乙酸钠,设计成微生物电池将氯苯转化为苯而除去,其原理如图所示。下列叙述正确的是
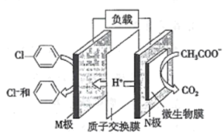
A.电子流向:N极→导线→M极→溶液→N极
B.M极的电极反应式为![]()
C.每生成lmlCO2,有3mole-发生转移
D.处理后的废水酸性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种新型电池放电时的总反应方程式为:![]() ,装置如图。下列说法正确的是
,装置如图。下列说法正确的是![]()

A.放电过程中![]() 通过膜向正极移动
通过膜向正极移动
B.右侧的电极反应式为:![]()
C.若M为Al,则电池放电过程的负极反应式为:![]()
D.在![]() 空气电池中,为防止负极区沉积
空气电池中,为防止负极区沉积![]() ,可改用稀硫酸做电解质溶液
,可改用稀硫酸做电解质溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,浓度均为0.2 mol·L-1的NaHCO3和Na2CO3溶液中,下列判断不正确的是( )
A.均存在电离平衡和水解平衡
B.存在的粒子种类不同
C.c(OH-)前者小于后者
D.分别加入NaOH固体,恢复到原温度,c(CO32-)均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)![]() 2C(g)+2D(g)在四种不同情况下的反应速率分别为:
2C(g)+2D(g)在四种不同情况下的反应速率分别为:
①v(A)=0.45mol/(Ls)
②v(B)=0.6mol/(L·s)
③v(C)==0.4mol/(L·s)
③v(D)=0.45mol/(Ls)
下列有关反应速率的比较中正确的是
A.④>③>②>①B.④<③=②<①C.①>②>③>④D.④>③=②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,相同pH的盐酸和醋酸溶液分别加水稀释,平衡pH随溶液体积变化的曲线如图所示。据图判断不正确的是
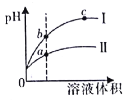
A.I是盐酸,II是醋酸
B.b点酸的总浓度大于a点酸的总浓度
C.溶液的导电性a>b>c
D.a、b、c三点KW的数值相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1100℃,一定容积的密闭容器中发生反应:FeO(s)+CO(g) ![]() Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
Fe(s)+CO2(g) △H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是( )
A. 若生成1 mol Fe,则吸收的热量小于a kJ
B. 若升高温度,正反应速率加快,逆反应速率减慢,则化学平衡正向移动
C. 若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
D. 达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO2)=0.0263 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向某容积恒定的密闭容器中充入1 mol N2、3 mol H2,经充分反应后达到如下平衡:N2(g)+3H2(g)![]() 2NH3(g),下列有关说法中正确的是( )
2NH3(g),下列有关说法中正确的是( )
A. 达平衡后再加入一定量的N2,体系内各物质含量不变
B. N2、H2、NH3的浓度一定相等
C. 反应没有达到平衡时,NH3会不断地分解,达到平衡时则不会再分解
D. 平衡时,N2、H2物质的量之比为1∶3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com