
100 mL 6 mol·L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量 ( )。
①Na2CO3(s) ②BaCl2(aq) ③Na2S(s) ④CH3COONa(s) ⑤KNO3(aq) ⑥H2O ⑦NaCl(aq)
A.①③④⑥ B.②④⑥⑦ C.②③④⑥ D.③④⑤⑦
科目:高中化学 来源: 题型:
在下列各说法中,正确的是( )
A.ΔH>0表示放热反应,ΔH<0表示吸热反应
B.热化学方程式中的化学计量数只表示物质的量,可以是分数
C.1 mol H2SO4与1 mol Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热
D.1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度时,将1 mol A和2 mol B放入容积为5 L的某密闭容器中发生如下反应:A(s)+2B(g)  C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述不正确的是( )
C(g)+2D(g),经5 min后,测得容器内B的浓度减少了0.2 mol/L。下列叙述不正确的是( )
A.在5 min 内该反应用C的浓度变化表示的反应速率为0.02 mol/(L·min)
B.5 min 时,容器内D的浓度为0.2 mol/L
C.该可逆反应随反应的进行,容器内压强逐渐增大
D.5 min时容器内气体总的物质的量为3 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
已知测定中和热的实验步骤如下:①量取50mL 0.25 mol/L硫酸倒入小烧杯中,测量温度; ②量取50mL 0.55mol/L NaOH溶液,测量温度; ③将NaOH溶液倒入小烧杯中,混合均匀后测量混合液温度。请回答:
(1)NaOH溶液稍过量的原因 。
(2)加入NaOH溶液的正确操作是 (填字母)。
A.沿玻璃棒缓慢加入 B.一次迅速加入 C.分三次加入
(3)使硫酸与NaOH溶液混合均匀的正确操作是 。
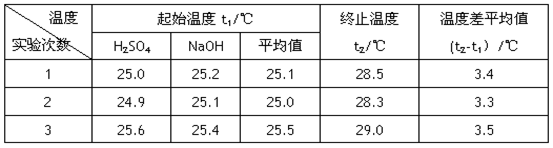
(4)设溶液的密度均为1g·cm-3,中和后溶液的比热c=4.18J·(g·℃)-1,请根据实验数据求出中和热为 ,写出该反应的热化学方程式_________
(5)若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量 (填“小于”、“等于”或“大于”)57.3 kJ,
查看答案和解析>>
科目:高中化学 来源: 题型:
有一真空瓶质量为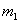 ,该瓶充入空气后质量为
,该瓶充入空气后质量为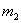 。在相同状况下,若改为充入某气体A时,总质量为
。在相同状况下,若改为充入某气体A时,总质量为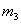 。则A的相对分子质量是( )
。则A的相对分子质量是( )
A.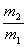 ×29 B.
×29 B.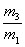 ×29 C.
×29 C.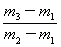 ×29 D.
×29 D.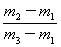 ×29
×29
查看答案和解析>>
科目:高中化学 来源: 题型:
下列既属于氧化还原反应,又属于吸热反应的是( )
A.铝片与稀盐酸反应 B.Ba(OH)2•8H2O与NH4Cl的反应
C.灼热的炭与水蒸气的反应 D.甲烷(CH4)在O2中的燃烧反应
查看答案和解析>>
科目:高中化学 来源: 题型:
①等物质的量的CO和CO2所含原子个数比为 ,质量比为 。
②含硫原子数相同的SO2和SO3的物质的量之比是 ;含氧原子数相同的SO2
和SO3的质量之比是 ,物质的量之比是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com