
【题目】(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子个数之比为________;氧原子个数之比为________;相同条件下体积比为________。
(2)某气体氧化物的化学式为RO2,在标准状况下,0.92g该氧化物的体积为448ml,则该氧化物的摩尔质量为________,R的相对原子质量为________。RO2的化学式为_____________
(3)常温下,在27.5g水中溶解12.5gCuSO4·5H2O,恰好达到饱和,该溶液的密度为1.21 g/cm3,则该溶液中CuSO4的物质的量浓度_________________,从中取出20.0 mL该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是_____________ml。
【答案】
(1)5:5:4;10:5:4 5:5:4
(2)46g/mol;14;NO2;
(3)1.51mol/L;30.2mL。
【解析】
试题分析:(1)质量比为16:7:6的三种气体 SO2、CO、NO物质的量之比为![]() :
:![]() :
:![]() =5:4:4,故三者分子数目之比为5:4:4,含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下,气体体积之比等于其物质的量之比,则三者体积之比为5:4:4,故答案为:5:5:4;10:5:4;5:5:4;
=5:4:4,故三者分子数目之比为5:4:4,含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下,气体体积之比等于其物质的量之比,则三者体积之比为5:4:4,故答案为:5:5:4;10:5:4;5:5:4;
(2)RO2的物质的量的物质的量为![]() =0.02mol,其摩尔质量为
=0.02mol,其摩尔质量为![]() =46g/mol,R的相对原子质量为46-32=14,R为N元素,RO2的化学式为NO2,故答案为:46g/mol;14;NO2;
=46g/mol,R的相对原子质量为46-32=14,R为N元素,RO2的化学式为NO2,故答案为:46g/mol;14;NO2;
(3)12.5g CuSO45H2O的物质的量为![]() =0.05mol,则溶液中硫酸铜的物质的量为0.05mol,溶液的体积为
=0.05mol,则溶液中硫酸铜的物质的量为0.05mol,溶液的体积为![]() =
=![]() mL,故硫酸铜溶液的物质的量浓度为
mL,故硫酸铜溶液的物质的量浓度为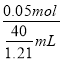 =1.51mol/L,根据稀释定律,稀释前后溶质的物质的量不变,则20.0ml该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积为
=1.51mol/L,根据稀释定律,稀释前后溶质的物质的量不变,则20.0ml该溶液,配成浓度为1.00mol/L的稀溶液,则稀释后溶液的体积为![]() =30.2mL,故答案为: 1.51mol/L;30.2mL。
=30.2mL,故答案为: 1.51mol/L;30.2mL。


科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. NH3比PH3稳定
B. S2-的离子半径比Cl-离子半径大
C. 第3周期元素中,金属性最强的是Na,非金属性最强的是Cl
D. 第ⅡA元素中,Be是化学性质最活泼的金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是( )
A.CaCO3 (s)=CaO(s)十CO2(g)室温下不能自发进行,说明该反应的△H<0
B.镀锌铁制品镀层受损后,铁制品比受损前更容易生锈
C.生铁中含有碳,抗腐蚀能力比纯铁强
D.Zn具有还原性和导电性,可用作碱性锌锰干电池的负极材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家刚刚发现了某种元素的原子,其质量是a g,12C的原子质量是b g,NA是阿伏加德罗常数的值,下列说法不正确的是
A.由已知信息可得:NA=![]() B.Wg该原子的物质的量一定是
B.Wg该原子的物质的量一定是 ![]() mol
mol
C.Wg该原子中含有![]() 个该原子g D.该原子的摩尔质量是aNA g
个该原子g D.该原子的摩尔质量是aNA g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】唐代诗人杜牧有首诗为“银烛秋光冷画屏,轻罗小扇扑流萤。天街夜色凉如水,卧看牵牛织女星。”,其中的流萤是指飞舞的萤火虫,萤火虫发光所需的能量直接来自于 ( )
A.C6H12O6的分解 B.蛋白质的分解
C.ATP的水解 D.脂肪的分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以物质的量为中心的相关计算,已知阿伏伽德罗常数为NA.
(1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是___________,在相同温度和相同压强条件下,体积最大的是___________。
(2)73.0g HCl气体中含有_______个分子、________个原子、______个质子、_________个电子,标况下体积约为_______L
(3)23.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为________, MCl2的相对分子质量为________,M的相对原子质量为________。
(4)将0.5L1mol/L FeCl3溶液加水稀释至1L,所得溶液中氯离子的物质的量浓度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校化学研究性学习小组的同学探究以铜为电极电解电解质溶液的情况,
第一组同学以铜为电极电解饱和食盐水,探究过程如下:
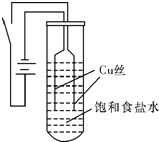
【实验Ⅰ】如图装置,电源接通后,与电池负极相连的铜丝上有大量气泡产生;与电池正极相连的铜丝由粗变细.电解开始30s内,阳极附近出现白色浑浊,然后开始出现橙黄色浑浊,此时测定溶液的pH约为10;随着沉淀量的逐渐增加,橙黄色沉淀慢慢聚集在试管底部,但溶液始终未出现蓝色。
【实验Ⅱ】将实验Ⅰ中试管底部的橙黄色沉淀取出,分装在两支小试管中,沉淀很快转变为砖红色,后续的操作及现象如下:

请回答下列问题:
(1)聚集在试管底部的橙黄色沉淀的化学式为______________.
(2)阳极的电极反应式为______________.
(3)写出实验Ⅱ中①、②的离子方程式:①__________;②__________.
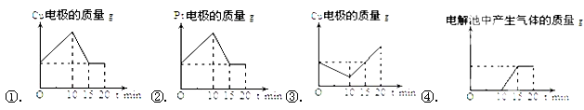
(4)第二组同学将质量相等的铜片和铂片插入硫酸铜溶液中,铜片与电源正极相连铂片与电源负极相连,以电流强度1A通电10min,然后反接电源,以电流强度2A继续通电10min.画出下列表示铜电极、铂电极、电解池中产生气体的质量和电解时间的关系图,其中正确的是( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com