
某有机物的结构简式如下图所示(未表示出其空间构型)。下列关于该物质的性质描述不正确的是( )
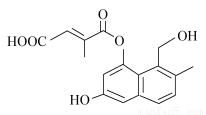
A.能使酸性KMnO4溶液褪色
B.能与FeCl3溶液发生显色反应
C.既能发生消去反应,也能发生取代反应
D.1 mol该物质最多可与5 mol NaOH反应
科目:高中化学 来源:2014高考化学苏教版总复习 专题1化学家眼中的物质世界练习卷(解析版) 题型:选择题
有如下反应:①H2S+H2O2=S↓+2H2O
②S+O2=SO2 ③SO2+Br2+H2O=HBr+H2SO4
下列物质的氧化性强弱判断正确的是( )
A.H2O2>S O2>SO2 B.H2O2>O2 Br2>O2
C.Br2>H2O2 SO2>S D.Br2>H2O2 Br2>SO2
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:选择题
下面有关晶体的叙述中,不正确的是( )
A.金刚石为网状结构,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题11有机化学基础练习卷(解析版) 题型:填空题
化合物A是合成天然橡胶的单体,分子式为C5H8。A的一系列反应如下(部分反应条件略去):

回答下列问题:
(1)A的结构简式为________,化学名称是________;
(2)B的分子式为________;
(3)②的反应方程式为________;
(4)①和③的反应类型分别是________,________;
(5)C为单溴代物,分子中有两个亚甲基,④的化学方程式为________;
(6)A的同分异构体中不含聚集双烯(CCC)结构单元的链状烃还有________种,写出其中互为立体异构体的化合物的结构简式:________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题11有机化学基础练习卷(解析版) 题型:选择题
2,2,4?三甲基戊烷与氯气发生取代反应时,生成的一氯代物可能有( )
A.2种 B.3种 C.4种 D.5种
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题10化学实验基础练习卷(解析版) 题型:实验题
化学兴趣小组设计以下实验方案,测定某已部分变质的小苏打样品中Na2CO3的质量分数。
方案一:称取一定质量样品,置于坩埚中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)坩埚中发生反应的化学方程式为:________。
(2)实验中,需加热至恒重的目的是________。
方案二:称取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。(已知:Ba2++OH-+HCO3—=BaCO3↓+H2O)
(1)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为________。
(2)实验中判断沉淀是否完全的方法是________。
方案三:按如下图所示装置进行实验:
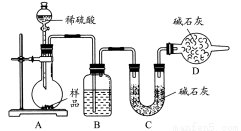
(1)D装置的作用是________。分液漏斗中________(填“能”或“不能”)用盐酸代替稀硫酸进行实验。
(2)实验前称取17.90 g样品,实验后测得C装置增重8.80 g,则样品中Na2CO3的质量分数为________。
(3)根据此实验测得的数据,测定结果有误差,因为实验装置还存在一个明显缺陷,该缺陷是________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题10化学实验基础练习卷(解析版) 题型:选择题
关于下列各实验装置的叙述中,正确的是( )

A.装置①制备乙酸乙酯
B.装置②中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
C.装置③可用于干燥、收集Cl2,并吸收多余的Cl2
D.装置④配制一定物质的量浓度的溶液时转移液体
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师高考模拟演练练习卷(B)(解析版) 题型:填空题
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%。
(1)有效减碳的手段之一是节能,下列制氢方法最节能的是 。
A.电解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O CO+3H2
CO+3H2
(2)CO2可转化成有机物实现碳循环。在体积为1 L 的密闭容器中,充入1 mol CO2和3 mol H2,一定条件下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
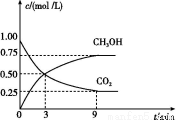
①从3 min到9 min,v(H2)= mol/(L·min)。
②能说明上述反应达到平衡状态的是 (填编号)。
A.反应中CO2与CH3OH的物质的量浓度之比为1∶1(即图中交叉点)
B.混合气体的密度不随时间的变化而变化
C.单位时间内消耗3 mol H2,同时生成1 mol H2O
D.CO2的体积分数在混合气体中保持不变
(3)工业上,CH3OH也可由CO和H2合成。参考合成反应CO(g)+2H2(g) CH3OH(g)的平衡常数:
CH3OH(g)的平衡常数:
温度/℃ | 0 | 100 | 200 | 300 | 400 |
平衡常数 | 667 | 13 | 1.9×1 | 2.4×1 | 1×1 |
下列说法正确的是 。
A.该反应正反应是放热反应
B.该反应在升高温度时,CH3OH(g)的体积分数减小,说明v正(CH3OH)减小,v逆(CH3OH)增大
C.在T ℃时,1 L密闭容器中,投入0.1 mol CO和0.2 mol H2,达到平衡时,CO转化率为50%,则此时的平衡常数为100
D.工业上采用稍高的压强(5 Mpa)和250 ℃,是因为此条件下,原料气转化率最高
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 电解质溶液练习卷(解析版) 题型:选择题
将铁铝矾[Al2Fe(SO4)4·xH2O]溶于水中,得到浅绿色溶液,有关该溶液的叙述正确的是( )
A.铁铝矾有净水作用,其水溶液显中性
B.该溶液中:2c(Al3+)+c(Fe2+)+c(H+)=4c(S )+c(OH-)
)+c(OH-)
C.在空气中,该溶液蒸干并灼烧,最后所得的残留固体为Al2O3、Fe2O3
D.向该溶液中加入Ba(OH)2溶液,当S 完全沉淀时,Al3+、Fe2+恰好被完全沉淀
完全沉淀时,Al3+、Fe2+恰好被完全沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com