
| A. | 篮球架的表面喷涂油漆,主要是为了美观 | |
| B. | 回收金属饮料罐,只是为了减少环境污染 | |
| C. | 银的导电性比铜好,所以常用银作电线而不用铜 | |
| D. | 不锈钢抗腐蚀性好,常用于制医疗器械、炊具等 |
分析 A.篮球架的表面喷涂油漆,不只是为了美观主要的是防锈;
B.回收金属饮料罐,可以节约金属资源;
C.银的导电性比铜好,但是银的价格比铜高;
D.根据合金不锈钢的知识进行分析,不锈钢抗腐蚀性好,常用于制炊具、医疗器械等;
解答 解:A.篮球架的表面喷涂油漆能隔绝空气和水,主要是为了防止金属生锈,故A错误;
B.回收金属饮料罐,可以再利用金属,节约金属资源,故B错误;
C.银的导电性比铜好,但是银的价格较高,所以银一般不用作导线.故C错误;
D.不锈钢是由铁、铬、镍制成的,具有强的抗腐蚀性能,常用于制医疗器械、炊具等,故D正确;
故选D.
点评 本题考查了金属的知识,在考虑物质的用途时,不但要考虑物质的性质,还要考虑其它方面的影响,掌握各种物质的性质方面的知识是解答关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
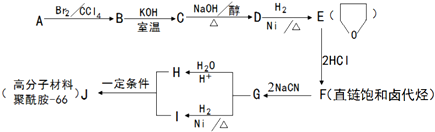
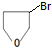 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$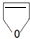 +NaBr+H2O.
+NaBr+H2O.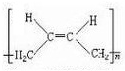 .
.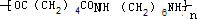 +2nH2O.
+2nH2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
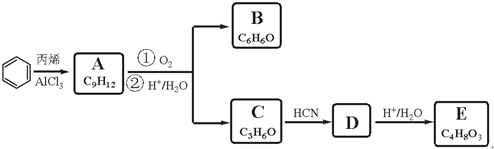
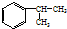 ,A的含有苯环的同分异构体(除A外)有7种.
,A的含有苯环的同分异构体(除A外)有7种.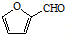 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂,写出该反应的化学方程式 .
. G:
G: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4 L Cl2完全溶于氢氧化钠溶液时,转移电子数为NA | |
| B. | 常温下,1 L pH=1的H2SO4溶液中含有的H+的数目为0.2NA | |
| C. | 标准状况下,2.24 L NH3中含有共价键的数目为0.3NA | |
| D. | 常温下,22.4 L NO2和N2O4的混合气体中含有NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

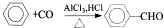
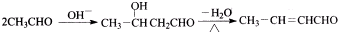
 .
.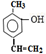 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
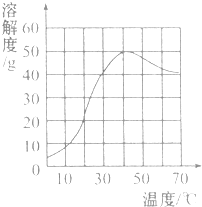
| A. | 硫酸钠的溶解度随温度升高而增大 | |
| B. | 30℃时硫酸钠饱和溶液的质量分数为40% | |
| C. | 40℃时硫酸钠的溶解度约为50g | |
| D. | 60℃时硫酸钠饱和溶液降温后一定饱和 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
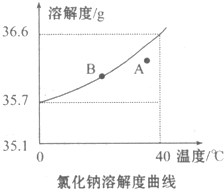 根据氯化钠的溶解度曲线,完成下列问题.
根据氯化钠的溶解度曲线,完成下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤经过气化和液化两个物理变化,可变为清洁能源 | |
| B. | 新型生物柴油和矿物油主要化学成分相同 | |
| C. | “洁厕灵”有效成分为盐酸,与漂白粉混合使用效果更佳 | |
| D. | 用银器盛放鲜牛奶,溶入的极微量的银离子,可杀死牛奶中的细菌,防止牛奶变质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com